Etilacetāts
| Etilacetāts | |
|---|---|
 | |
| CAS numurs | 141-78-6 |
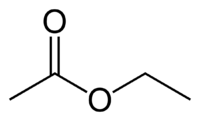
| Ķīmiskā formula | CH3COOCH2CH3 |
| Molmasa | 88,105 g/mol |
| Blīvums | 897 kg/m3 |
| Kušanas temperatūra | −83,6 °C (189,55 K) |
| Viršanas temperatūra | 77,1 °C (350,25 K) |
Etilacetāts (etiķskābes etilesteris, CH3COOCH2CH3) ir bezkrāsains, gaistošs šķidrums ar patīkamu smaržu. To lielākoties lieto par šķīdinātāju. Etilacetāts ir esteris un to iegūst no etiķskābes un etanola. Etilacetāts nav higroskopisks un ūdenī šķīst slikti. Istabas temperatūrā etilacetāta šķīdība ūdenī ir 8% un ūdens šķīdība etilacetātā ir 3%. Paaugstinoties temperatūrai, šķīdība palielinās. Stipru skābju un bāzu klātienē etilacetāts sadalās.
Iegūšana[labot šo sadaļu | labot pirmkodu]
Etilacetātu var iegūt, etiķskābei reaģējot ar etanolu skābes katalizatora (parasti sērskābes) klātienē:
CH3CH2OH + CH3COOH → CH3COOCH2CH3 + H2O
Sērskābe šajā reakcijā piesaista ūdeni, lai reakcijas līdzsvaru nobīdītu estera rašanās virzienā.
Etilacetātu līdzīgā veidā var iegūt arī, etanolam reaģējot ar acetanhidrīdu vai hloracetanhidrīdu, šīs vielas pašas reaģē ar ūdeni, tāpēc sērskābes klātiene nav tik ļoti nepieciešama (hloracetanhidrīdam nevajag nemaz).
Etilacetātu var iegūt arī no acetaldehīda bāziska alkoksīda katalizatora klātienē. Šī ir viena no rūpnieciskajām etilacetāta ražošanas metodēm:
CH3CHO + CH3CHO → CH3COOC2H5
Vēl etilacetātu var iegūt, katalītiski dehidrogenējot etanolu. Šī ir viena no rūpnieciskajām etilacetāta ražošanas metodēm, bet to nelieto pārāk plaši, jo etanols ir salīdzinoši dārgs (to lieto, ja ir jāatbrīvojas no lieka etanola):
2CH3CH2OH → CH3COOC2H5 + 2H2
Šajā reakcijā veidojas daudz blakusproduktu (dietilēteris, acetaldehīds, citi esteri, ketoni), kas, tāpat kā etanols, veido azeotropus maisījumus ar ūdeni.
Ķīmiskās īpašības[labot šo sadaļu | labot pirmkodu]
Reaģējot ar skābēm un bāzēm, etilacetāts hidrolizējas par etanolu un etiķskābi. Skābes klātienē reakcija notiek nepilnīgāk kā bāzes klātienē, jo bāzes (sārmi) ar veidojušos etiķskābi veido acetātus, kas tālāk nevar izreaģēt ar etanolu, no jauna veidojot etilacetātu.
Izmantošana[labot šo sadaļu | labot pirmkodu]
Etilacetātu lieto par šķīdinātāju nagu lakām un dažreiz arī citām lakām un krāsām. Etilacetātu arī dažreiz lieto bezkofeīna kafijas ražošanai, kofeīna ekstrakcijai. Etilacetātu lieto par šķīdinātāju šķidruma hromatogrāfijai. Etilacetātu parasti nelieto par šķīdinātāju organisko sintēžu reakcijas maisījumiem, jo tas var hidrolizēties.
