Tritijs
Šim rakstam ir nepieciešamas atsauces uz ārējiem avotiem. Lūdzu, palīdzi uzlabot šo rakstu, pievienojot vismaz vienu atsauci. Ja ir kādi ieteikumi, vari tos pievienot diskusijā. Vairāk lasi lietošanas pamācībā. Meklēt atsauces: "Tritijs" – ziņas · grāmatas · scholar · brīvi attēli |
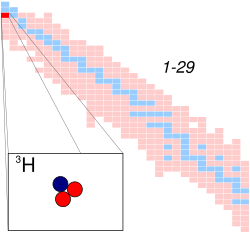
Tritijs (grieķu: τρίτος (tritos) — 'trešais, trešējais') jeb pārsmagais ūdeņradis ir trešais no ūdeņraža izotopiem. Tritijs ir nestabils izotops — tā kodola pussabrukšanas periods ir 12,32 gadi. Tritija apzīmējums ir 3H vai T. Tritija atoma kodols (tritons) sastāv no viena protona un diviem neitroniem.
Tritiju atklājuši angļu zinātnieki Ernests Rezerfords, Marks Olifants un Pauls Harteks.
Dabā tritijs veidojas, kosmisko staru daļiņām saduroties ar atmosfēras gāzu, piemēram, slāpekļa, atomu kodoliem. Mākslīgi rūpnieciskos mērogos tritiju iegūst, kodolreaktorā apstarojot litiju ar neitroniem:
- .
Tritiju var iegūt arī, apstarojot ar neitroniem smago ūdeni, jo deitērijs var satvert neitronu un pārvērsties par tritiju. ASV kopš 1955. gada ir iegūti apmēram 225 kg tritija.
Tritija kodols sabrūk, izstarojot elektronu un elektronu antineitrīno un rodoties hēlijam-3. Tā kā radusies elektronu plūsma (bēta stari) ir ar samērā nelielu enerģiju — vidēji ap 6 keV — tritiju lieto tehnikā un pat sadzīvē, jo tik mazas enerģijas bēta stari nespēj izkļūt cauri cilvēka ādai. Tomēr tritijs ir bīstams, to ieelpojot vai norijot.

Tritiju lieto bioloģijā un ķīmijā kā radioaktīvu marķieri. To lieto arī neitrīno īpašību pētīšanai un kodoltermiskajos ieročos kā neitronu avotu un vienlaicīgi kodoldegvielu (skatīt ūdeņraža bumba). Ar tritija savienojumiem (tiem jābūt pilnīgi negaistošiem — parasti lieto polimērus, kuros neliela daļa ūdeņraža aizstāta ar tritiju) aktivētus luminoforus lieto patstāvīgi spīdošu krāsu ražošanai, kuras izmanto pulksteņu ciparnīcu, kompasu, mērinstrumentu, šaujamieroču tēmēkļu pārklāšanai. Ar šādām krāsām aizstāj agrāk (apmēram līdz 20. gadsimta 60. gadiem) izmantotās rādiju un cinka sulfīdu saturošās krāsas, kas bija ļoti kaitīgas.
|

