Destilācija
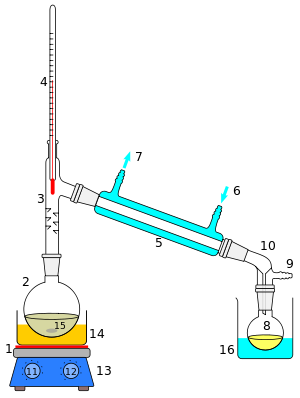
1 — siltuma avots (elektriskā plītiņa ar magnētisko maisītāju),
2 — destilācijas kolba,
3 — šlifa pāreja (Virca pāreja),
4 — pieslīpēts termometrs,
5 — Lībiga dzesinātājs,
6 — dzesējošā ūdens ieplūde,
7 — dzesējošā ūdens izplūde,
8 — destilāta savākšanas kolba,
9 — atzars vakuuma pieslēgšanai vai inertas gāzes ievadei,
10 — pieslīpēta novadule,
11 — temperatūras regulators,
12 — maisītāja apgriezienu regulators,
13 — vadības panelis,
14 — ūdens, eļļas vai smilšu vanna,
15 — vārķermeņi un magnētiskā maisītāja ampula,
16 — dzesēšanas vanna.
Destilācija (no latīņu: destillatio — 'pilēšana') jeb pārtvaice ir šķidru vielu (šķīdumu) maisījumu sadalīšanas metode, kas pamatojas uz vielu dažādu gaistamību dažādās temperatūrās. Destilācijas laikā šķidrums tiek iztvaicēts un vēlāk tā tvaiki atdzesēti un kondensēti.
Vēsture[labot šo sadaļu | labot pirmkodu]
Tiek uzskatīts, ka destilāciju izgudroja arābi pirms 10. gadsimta. Avicenna to min kā ēterisko eļļu iegūšanas metodi.
Destilācijas veidi[labot šo sadaļu | labot pirmkodu]
- Vienkārša destilācija ir verdoša šķidruma daļēja iztvaicēšana un radušos tvaiku kondensēšana dzesinātājā. Iegūto pārtvaices produktu sauc par destilātu, bet pārtvaicēšanai izmantoto iekārtu — par destilatoru. Neiztvaicēto šķidrumu sauc par destilācijas atlikumu. Vienkāršā destilācijā iegūst tikai vienu produktu.
- Frakcionētā destilācija ir vienkāršas destilācijas paveids šķidra daudzkomponentu maisījuma sadalīšanai vairākās atšķirīga sastāva daļās jeb frakcijās. Pamatojas uz zemākā temperatūrā virstošu vielu ātrāku iztvaikošanu un kondensēšanos, kamēr augstākā temperatūrā virstošas vielas kondensējas vēlāk. Frakcionēti destilējot, produktus savāc vairākos uztveršanas traukos noteiktos laika vai temperatūras intervālos.
- Destilācija ar deflegmāciju, kuru lieto labākai frakciju atdalīšanai, izmantojot deflegmatorus jeb virsmas kondensatorus. Deflegmatorā sākumā kondensējas grūtāk gaistošais šķidruma komponents, kamēr tvaiks, kas plūst uz augšu pa deflegmatoru, bagātinās ar vieglāk gaistošo komponentu.
- Destilācija ar ūdens tvaiku tiek izmantota, ja destilējamā viela nejaucas ar ūdeni. Destilējamam šķīdumam barbotē cauri ūdens tvaiku, tādējādi pazeminot destilācijas temperatūru. Pēc destilācijas nešķīstošo komponentu (piemēram, benzolu vai sēroglekli) atdala, nostādinot vai centrifugējot.
- Vakuuma destilāciju izmanto termiski nestabilu vai sevišķi grūti gaistošu vielu maisījumu sadalīšanai, jo vakuumā vielas vārās daudz zemākā temperatūrā.
- Azeotropā destilācija ir destilācijas veids, kuru izmanto azeotropu maisījumu sadalīšanai, pievienojot destilējamam maisījumam vielas, kas veido citu azeotropu maisījumu ar kādu no komponentēm.
Izmantošana[labot šo sadaļu | labot pirmkodu]

Lai destilācijas metode būtu pielietojama, šķidruma komponentu viršanas temperatūrām jābūt pietiekami atšķirīgām, turklāt destilējot nevar iegūt pilnīgi tīru produktu.
Destilāciju plaši izmanto ķīmiskajā, farmaceitiskajā, naftas pārstrādes rūpniecībā, kā arī ķīmiskajās laboratorijās. Ar destilācijas (vienkāršas vai vairākkārtējas) metodi tiek iegūti daudzu alkoholisku dzērienu (konjaka, ruma, viskija) pusfabrikāti, bet mājas apstākļos — kandža.
Destilāciju lieto arī ūdens attīrīšanai, iegūstot destilētu ūdeni.
Skatīt arī[labot šo sadaļu | labot pirmkodu]
Literatūra[labot šo sadaļu | labot pirmkodu]
- L. Osipovs. Ķīmijas tehnoloģijas pamatprocesi un aparāti. R:, Zvaigzne, 1991, 486.—490. lpp.
| Vikikrātuvē par šo tēmu ir pieejami multivides faili. Skatīt: Destilācija |
|
