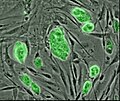
Cilmes šūna

Cilmes šūnas jeb mātšūnas ir nediferencētas šūnas, kādas ir visos daudzšūnu organismos, un tās var dalīties meitšūnās un diferencēties cita veida šūnās. Cilmes šūnas nodrošina organisma nemitīgu atjaunošanos. Visvairāk cilmes šūnu ir embrionālajā un zīdaiņa attīstības posmā, kad to uzdevums ir veidot orgānus. Arī zigota ir uzskatāma par cilmes šūnu. Ar laiku cilmes šūnu daudzums organismā samazinās, kas izskaidro organisma novecošanas procesu, jo tās nespēj atjaunot visas bojātās šūnas.
Zīdītājiem ir divu veidu cilmes šūnas: embrionālās cilmes šūnas, kuras ir izolētas no iekšējās šūnas masas (blastulas) un pieaugušo cilmes šūnas, kas ir atrodamas dažādos audos. Pieaugušiem organismiem, cilmes šūnas darbojas kā organisma remonta sistēma, papildinot jau pieaugušos audus. Embrionālajām cilmes šūnām var iedalīt visās specializēto šūnu kategorijās – ektoderma, endoderma un mezoderma, kā arī tās spēj uzturēt reģeneratīvo orgānu atjaunošanos, piemēram, asins, ādas vai zarnu audu.
Ir zināmi trīs veidi, kā iegūt autologas pieaugušo cilmes šūnas:
- Kaulu smadzenēs, veicot urbumu augšstilbā vai gūžas kaulā;
- Taukaudos, veicot tauku atsūkšanu;
- Asinīs, kur asinis tiek ņemtas no donora. Šajā procesā asinis tiek filtrētas caur īpašu ierīci un tiek iegūtas cilmes šūnas.
Cilmes šūnas var tikt noņemtas arī no nabassaites asinīm tikko pēc bērna dzimšanas. No visiem cilmes šūnu iegūšanas tipiem šis ir vismazāk bīstamākais, kā arī ir iespēja nodod šīs asinis asins bankā, lai nepieciešamības gadījumā tās varētu izmantot ķirurģiskām procedūrām.
Pieaugušo cilmes šūnas (jeb somatiskās) bieži tiek izmantotas dažādās medicīniskās terapijās (piemēram, kaulu smadzeņu transplantācijai). Mūsdienās cilmes šūnas var audzēt mākslīgi, kā arī pārveidot (diferencēt) uz šūnu tipiem ar īpašām šūnu īpašībām, kas atbilst šūnām dažādos audos, piemēram, muskuļu un nervu šūnas. Embrionālās cilmes šūnas, kas iegūtas izmantojot somatisko šūnu kodola pārvietošanu ir uzskatāma kā daudzsološa nākotnes terapija. Pētījumi par cilmes šūnu attīstību ir veidojušies no pētnieku Ernesta A. Makkuloča un E. Džeimsa Toronto Universitātē līdz 1960. gadam.[1]
Definīcija[labot šo sadaļu | labot pirmkodu]
Pēc klasiskās cilmes šūnu definīcijas var izdalīt divas būtiskas īpašības:
- Pašatjaunošanās: spēja sevi atjaunot ilgstošā laika periodā daloties
- Potence: noteiktos fizioloģiskos vai eksperimentālos apstākļos tās var ievirzīt uz specializētu šūnu veidošanu. Pluripotentiālas (embrionālās cilmes šūnas) spēj veidot visdažādākos audus. Savukārt, multipotentas (pieaugušo cilmes šūnas) spēj veidot vairākus audu tipus, taču to skaits ir būtiski ierobežots.
Pašatjaunošanās[labot šo sadaļu | labot pirmkodu]
Ir divi mehānismi, kas nodrošina cilmes šūnu veiksmīgu saglabāšanos:
- Obligāta asimetriska replikācija: cilmes šūna tiek sadalīta vienā mātes šūnā, kas ir identiska ar sākotnējo cilmes šūnu un ar citu meitas šūnu, kas ir diferencēta.
- Stohastiskā diferencēšana: notiek, kad viena cilmes šūna attīstās divās diferencētās meitas šūnās, kamēr cita cilmes šūna iziet mitozes ciklu un iegūst divas cilmes šūnas, kuras ir identiskas oriģinālam.
Cilmes šūnu potenciāls[labot šo sadaļu | labot pirmkodu]

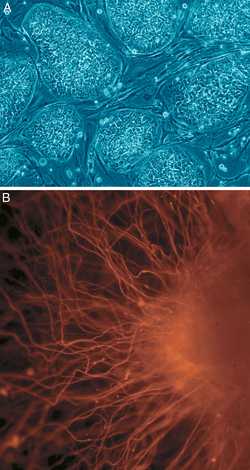
A: Cilmes šūnu kolonija, kura vēl nav diferencējusies.
B: Nervu, šūnu veids pēc diferencācijas.
Šūnas iedarbības stiprumu nosaka potenciāls diferencēt dažādus šūnu veidus no cilmes šūnām.[2]
- Totipotentas jeb omnipotentas cilmes šūnas ir apaugļotas olšūnas, no kurām var veidoties dažādi šūnu veidi – šādas šūnas var izveidot pilnīgu un dzīvotspējīgu organismu.[2] Šīs šūnas tiek veidotas apaugļošanas procesā. Šūnas, kas veidojušās morulas stadijā (pirmajās apaugļotas olšūnas šūnu dalīšanās stadijās) arī ir totipotentas.[3]
- Pluripotentas cilmes šūnas ir līdzīgas tolipotentām šūnām, t.i., šī šūnas var specializēties par jebkuru organismā sastopamo šūnu veidu. Šīs ir embrionālas cilmes šūnas, kuras var iegūt no piecas dienas apaugļotas blastocistas. Tās nevar pārvērsties atpakaļ par totipotentām šūnām.[4]
- Multipotentas cilmes šūnas spēj veidot vienas saimes jebkuras šūnas. Tās ir nediferencētas un atrodas audos un orgānos, piemēram, no mezodermas veidojot kaulu smadzenes, asinis un muskuļu šūnas. Tās nodrošina šūnu atjaunošanos visā dzīves garumā.[2]
- Oligopotentas cilmes šūnas var diferencēt tikai dažos šūnu tipos, piemēram, limfoīdām vai mieloīdām šūnām.[2]
- Unipotentas cilmes šūnas ir sastopamas pēdējos zigotas attīstības posmos, tās spēj diferencēties tikai par vienu šūnu veidu, taču salīdzinot ar pieaugušām šūnām, šīs šūnas ir spējīgas dalīties.[2]
Šūnu identificēšana[labot šo sadaļu | labot pirmkodu]
Praksē, cilmes šūnas tiek identificētas pēc tā, vai tās spēj atjaunot audus. Piemēram, veicot testus kaulu smadzenēs vai asinsrades cilmes šūnās (HSC) ir iespējams veikt šūnu transplantāciju bez HSC. Tas parāda to, ka šūnas spēj ražot jaunas asins šūnas ilgākā laika posmā. Tāpat būtu iespējams izolēt cilmes šūnas no indivīda, kuram ir veikta šo šūnu transplantācija un transplantēt tās citam indivīdam bez HSC, kas parāda to, ka cilmes šūnas ir spējīgas pašas atjaunoties.[5][6]
Embrionālās šūnas[labot šo sadaļu | labot pirmkodu]
Embrija cilmes šūnas ir šūnas no blastocistas iekšējās šūnu masas, kas ir agrīnā embrija stadija.[7] Cilvēka embrijs blastocistas stadiju sasniedz 4—5 dienas pēc apaugļošanas, kad tā sastāv no 50—150 šūnām. Embrionālās cilmes šūnas ir pluripotentas un spēj diferencēties par jebkuru no trim cilvēka primārās dzimumšūnas slāņiem: ektodermu, endodermu un mezodermu. Kas nozīmē to, ka šīs šūnas var izvērsties par jebkuru no vairāk nekā 200 šūnu tipiem pieauguša cilvēka ķermenī, kad tiek dota pietiekama stimulācija konkrētajām šūnām tipam. Taču šīs šūnas nespēj veidot ārpus embrionālu membrānu vai placentu. Embrionālās attīstības laikā, iekšējās šūnas masas šūnas pastāvīgi dalās un kļūst arvien specializētākas. Piemēram, daļa no embrija ektodermas muguras daļā specializējas kā „neiroektoderma”, kas nākotnē pārveidosies par centrālo nervu sistēmu.[8] Tālākā posmā neiroektoderma veidosies par neironu caurulīti. Nervu caurulītes veidošanās posmā, tiek veidota galvenā smadzeņu forma. Šajā attīstības stadijā, galvenais CNS šūnu tips tiek uzskatītas nervu cilmes šūnas. Šīs neironu cilmes šūnas ir pluripotentas, jo tās spēj veidot lielu dažādību daudziem, dažādiem neironu tipiem, kur katram var būt unikāla gēnu ekspresija, morfoloģiskās un funkcionālās īpašības. Process, kurā tiek ģenerēti neironi no cilmes šūnām tiek saukti par neiroģenēzi. Izcils piemērs ir nervu cilmes šūnas, kuras ir gliālas šūnas, tāpēc, ka tām ir atšķirīga bipolārā morfoloģija. Glijas šūnas ir vissvarīgākās neirālās cilmes šūnas, lai mugurkaulniekiem attīstītos CNS. Neironu cilmes šūnas ir piederīgas pie neironu ciltskoka (neironi, astroglijas un oligodendroīdi), tāpēc šo šūnu iedarbība un potenciāls ir ierobežots.[7] Gandrīz visi līdz šim veiktie pētījumi ir izmantojuši peles embrija cilmes šūnu (mES) vai cilvēka embrija cilmes šūnu (HES), kas iegūtas no agrīnās iekšējās šūnu masas. Abiem šūnu iegūšanas veidiem piemīt būtiskas cilmes šūnu īpašības, taču ir nepieciešamas atšķirīgas vides, lai saglabātu šūnas nediferencētā stāvoklī. Peles embrionālās šūnas tiek audzētas uz želatīna kārtiņas, kā ārpusšūnas matrica. Cilvēku embrionālās šūnas tiek audzētas peļu embrija fibroblastu apgādes slānī (MEF) šis process prasa pamata fibrolastu augšanas faktora klātbūtni (bFGF vai FGF-2).[9] Without optimal culture conditions or genetic manipulation,[10] Izmantojot cilvēka embrionālās cilmes šūnas laboratorijas apstākļos, lai veidotu specializētas šūnas kā nervu šūnas vai sirds šūnas, zinātnieki var piekļūt pieaugušu cilvēku šūnām bez audu ņemšanas no pacientiem. Zinātnieki var pētīt šīs specializētās pieaugušās šūnas detalizētāk, lai atrastu un pamanītu slimību komplikācijas vai pētīt šūnu reakciju uz potenciāli jaunām zālēm.[11] Pirmais izmēģinājums uz cilvēkiem apstiprināja ASV Pārtikas un Zāļu Administrācija, 2009. gada janvārī,[12] tomēr īstie pētījumi sākās tikai 2010. gada oktobrī, Atlantā, kur tika veikta muguras smadzeņu izpēte.[13] Balstoties uz ētiskiem apsvērumiem daudzās valstīs šobrīd ir moratorija vai ierobežojumi, gan cilvēku embrionālo šūnu izpētē, gan producēt jaunas embrionālās cilvēku šūnas. Balstoties uz embrionālo cilmes šūnu kombinētajām spējām uz neierobežotu pavairošanu, šīs šūnas teorētiski ir liels avots potenciālajai reģeneratīvās medicīnas un audu transplantācijai pēc traumas vai slimības attīstībai.[14]
-
Peles cilmes šūnas, kuras iekrāsotas ar fluorescences marķieri
-
Cilvēka embrionālo cilmes šūnu kolonija peles fibroblastu slānī
Embrija cilmes šūnas[labot šo sadaļu | labot pirmkodu]
Primitīvās cilmes šūnas ir izvietotas embrija orgānos, kas tiek sauktas par embrija cilmes šūnām.[15] Tiek iedalītas divu veidu embrija cilmes šūnas:
- Atbilstoši iegūtas embrija cilmes šūnas nāk no embrija pēc aborta veikšanas. Cilmes šūnas nav nemirstīgas un multipotentas.
- Ārpus embrija cilmes šūnas, kuras parasti nav atšķiramas no pieaugušo cilmes šūnām. Šīs cilmes šūnas tiek iegūtas pēc dzimšanas, tām ir augsta šūnu dalīšanās un pluripotentāte, taču tās ir mirstīgas.[16]
Pieaugušo cilmes šūnas[labot šo sadaļu | labot pirmkodu]
Pieaugušo cilmes šūnas, ko sauc arī par somatiskajām (no grieķu valodas σωματικóς (somatikos) — 'no ķermeņa'). Šīs cilmes šūnas uztur veic „remontdarbus” tajos audos, kuros ir atrastas cilmes šūnas.[17] Šīs cilmes var būt gan bērnos, gan pieaugušajos.[18] Pluripotentas pieaugušo cilmes šūnas ir reti sastopamas, taču parasti to skaits ir ļoti neliels, bet tās var atrast nabassaites asinīs un citos audos.[19] Kaulu smadzenes ir avots, kurā ir bagātīgi atrodamas pieaugušo cilmes šūnas,[20] kas tiek izmantotas dažādu slimību ārstēšanai, tostarp aknu cirozi,[21] hronisku ekstremitāšu išēmiju [22] un sirds mazspēju.[23] Kaulu smadzeņu cilmes šūnu daudzums samazinās ar vecumu un reproduktīvajā vecumā ir lielāks vīriešiem nekā sievietēm.[24] Daudzi pētījumi par pieaugušo cilmes šūnām ir centušies raksturot to potences un pašatjaunošanās spējas.[25] DNS bojājums uzkrājas ar vecumu gan cilmes šūnas, gan šūnās, kas ietver cilmes šūnu vidi. Šie bojājumi tiek uzskatīti par vismaz daļēju iemeslu, kāpēc palielinās cilmes šūnu disfunkcija un novecošana.[26] Pieaugušo cilmes šūnu terapija ir veiksmīgi izmantota jau vairākus gadus, lai ārstētu leikēmiju un ar to saistītās kaulu / asins vēža kaulu smadzeņu transplantāciju. [35] Pieaugušo cilmes šūnas tiek izmantotas arī veterinārijā, lai ārstētu cīpslu un saišu traumas zirgiem.[27] Pieaugušo cilmes šūnu izmantošana pētījumos un terapijā nav tik strīdīgs, jo to iegūšanai un izmantošanai nav nepieciešama embrija iznīcināšana. Gadījumos, kad pieaugušo cilmes šūnas tiek iegūtas no saņēmēja risks, ka organismā tās tiks noraidītas būtībā neeksistē. Tādēļ ASV valdība ir finansējusi pieaugušo cilmes šūnu pētniecību.[28]
Augļūdeņi[labot šo sadaļu | labot pirmkodu]
Multipotentas cilmes šūnas ir atrodamas arī augļūdeņa šidrumā. Šīs cilmes šūnas ir ļoti aktīvas, tām ir raksturīga aktīva attīstība bez barotavas un tās nav tumorogēnas. Augļūdeņu cilmes šūnas šobrīd ir aktīvā izpētē.[29] Izmantojot cilmes šūnas no augļūdeņa tiek pārvarētas ētikas normas un iebildumi par to, jo Romas katoļu baznīca ir aizliegusi izmantot embriju cilmes šūnas eksperimentāliem nolūkiem. Vatikāna laikrakstā „Osservatore Romano” augļūdeņu cilmes šūnas tiek sauktas par „nākotnes medicīnu”.[30] Mūsdienās ir iespējams savākt un uzglabāt augļūdeņu šūnas no donoriem vai autologai lietošanai [31][32]: Pirmā ASV augļūdeņu cilmes šūnu banka tika atvērta 2009. gada Medfordā, MA, to atvēra Biocell Center Corporation [33][34][35] un tā sadarbojas ar dažādām slimnīcām un universitātēm visā pasaulē.[36]
Izcelšanās[labot šo sadaļu | labot pirmkodu]
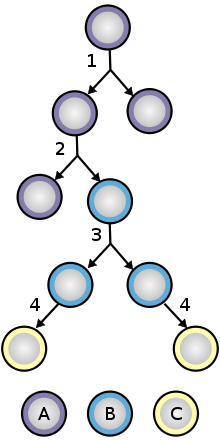
Lai cilmes šūnas pašas spētu nodrošināt pašatjaunošanos, tās iziet divu veidu dalīšanos (skat. Cilmes šūnu dalīšanās un diferenciācijas diagrammu). Simetriskā dalīšanās rada divas meitšūnas, kuras ir gan vienādas, gan apveltītas ar visām cilmes šūnas īpašībām. No otras puses, asimetriskais sadalījums rada tikai vienu cilmes šūnu un ierobežo tās pašatjaunošanās potenciālu. Cilmes šūnas var iet caur vairākkārtīgu šūnu dalīšanos pirms tās diferencējas par nobriedušu šūnu.[37]
Ārstēšana[labot šo sadaļu | labot pirmkodu]
Cilmes šūnu terapijā tiek izmantotas cilmes šūna, lai ārstētu vai novērstu slimības. Kaulu smadzeņu transplantācija ir vienīgā transplantācijas forma, kas tiek plaši izmantota.[38][39]
Trūkumi[labot šo sadaļu | labot pirmkodu]
Lai tiktu veikta ārstēšana ar cilmes šūnu palīdzību varētu būt nepieciešams veikt imūnsupresiju (jālieto vielas, kas nomāc organisma imunitāti), jo pirms transplantācija tiek veikta radiācija, lai atbrīvotos no pacienta iepriekšējām šūnām vai, lai to imūnsistēma neiznīcinātu ievadītās cilmes šūnas. Pieeja, lai izvairītos no tā, ka imūnsistēma nepieņem jaunās cilmes šūnas ir izmantot cilmes šūnas no tā paša pacienta, kurš tiek ārstēts. Pluripotentas atsevišķas cilmes šūnu konkrētu veidu ir grūti iegūt, jo to populācija ir diverencēta nevienērīgi.[40] Dažas cilmes šūnas pēc transplantācijas var veidot audzējus; pluripotentas šūnas ir saistītas ar audzēju veidošanos, jo īpaši embrija cilmes šūnas.[41]
Ārstēšana[labot šo sadaļu | labot pirmkodu]
- Slimības un diagnozes, kad cilmes šūnu terapija tiek izmantota:
- Diabēts
- Reimatoīdais artrīts
- Parkinsona slimība
- Alcheimera slimība
- Osteoartrīts[42]
- Insults un smadzeņu traumas[43]
- Mācīšanās darba nespēja, kas radīti iedzimtu traucējumu iedarbībā[44]
- Muguras smadzeņu trauma[45]
- Sirds infarkts[46]
- Pret vēža ārstēšana[47]
- Plikpaurība[48]
- Aizvietot trūkstošos zobus[49]
- Uzlabo dzirdi[50]
- Atjaunot redzi[51] un kaitējumu radzenei[52]
- Amiotrofiskā laterālā skleroze[53]
- Krona slimība [54]
- Brūču dzīšana[55]
- Vīriešu neauglība jo nav spermatogonālo cilmes šūnu.[56]
Pētījumi ir veikti, lai izstrādātu un attīstītu ārstēšanu ar cilmes šūnu palīdzību – neirodeģeneratīvās slimībs, diabēts, sirds slimības un citi apstākļi.
Atsauces[labot šo sadaļu | labot pirmkodu]
- ↑ Tuch BE (2006). "Stem cells—a clinical update". Australian Family Physician 35 (9): 719–21. PMID 16969445.
- ↑ 2,0 2,1 2,2 2,3 2,4 Schöler, Hans R. «The Potential of Stem Cells: An Inventory». In Nikolaus Knoepffler, Dagmar Schipanski, Stefan Lorenz Sorgner. Humanbiotechnology as Social Challenge. Ashgate Publishing, 2007. 28. lpp. ISBN 978-0-7546-5755-2.
- ↑ Mitalipov S, Wolf D (2009). "Totipotency, pluripotency and nuclear reprogramming". Adv. Biochem. Eng. Biotechnol.. Advances in Biochemical Engineering/Biotechnology 114: 185–99. Bibcode 2009esc..book..185M. doi:10.1007/10_2008_45. ISBN 978-3-540-88805-5. PMC 2752493. PMID 19343304.
- ↑ Ulloa-Montoya F, Verfaillie CM, Hu WS (2005). "Culture systems for pluripotent stem cells". J Biosci Bioeng. 100 (1): 12–27. doi:10.1263/jbb.100.12. PMID 16233846.
- ↑ Friedenstein AJ, Deriglasova UF, Kulagina NN, Panasuk AF, Rudakowa SF, Luriá EA, Ruadkow IA (1974). "Precursors for fibroblasts in different populations of hematopoietic cells as detected by the in vitro colony assay method". Experimental Hematology 2 (2): 83–92. ISSN 0301-472X. PMID 4455512.
- ↑ Friedenstein AJ, Gorskaja JF, Kulagina NN (1976). "Fibroblast precursors in normal and irradiated mouse hematopoietic organs". Experimental Hematology 4 (5): 267–74. PMID 976387.
- ↑ 7,0 7,1 Scott F. Gilbert, Swarthmore College, the University of Helsinki. Developmental biology (Tenth izd.). Sunderland, Mass. : Sinauer, 2014. ISBN 978-0878939787.
- ↑ Rakic, P (October 2009). "Evolution of the neocortex: a perspective from developmental biology". Nature reviews. Neuroscience 10 (10): 724–35. doi:10.1038/nrn2719. PMC 2913577. PMID 19763105.
- ↑ «Culture of Human Embryonic Stem Cells (hESC)». National Institutes of Health. Arhivēts no oriģināla, laiks: 2010-01-06. Skatīts: 2010-03-07.
- ↑ Chambers I, Colby D, Robertson M, Nichols J, Lee S, Tweedie S, Smith A (2003). "Functional expression cloning of Nanog, a pluripotency sustaining factor in embryonic stem cells". Cell 113 (5): 643–55. doi:10.1016/S0092-8674(03)00392-1. PMID 12787505.
- ↑ Boyer LA, Lee TI, Cole MF, Johnstone SE, Levine SS, Zucker JP, Guenther MG, Kumar RM, Murray HL, Jenner RG, Gifford DK, Melton DA, Jaenisch R, Young RA (2005). "Core transcriptional regulatory circuitry in human embryonic stem cells". Cell 122 (6): 947–56. doi:10.1016/j.cell.2005.08.020. PMC 3006442. PMID 16153702.
- ↑ Ron Winslow (2009). "First Embryonic Stem-Cell Trial Gets Approval from the FDA". The Wall Street Journal. 23 January 2009.
- ↑ «Embryonic Stem Cell Therapy At Risk? Geron Ends Clinical Trial». ScienceDebate.com. Arhivēts no oriģināla, laiks: 2014-08-22. Skatīts: 2011-12-11.
- ↑ Trounson, Alan; DeWitt, Natalie D. (23 February 2016). "Pluripotent stem cells progressing to the clinic". Nature Reviews Molecular Cell Biology 17: 194–200. doi:10.1038/nrm.2016.10.
- ↑ Ariff Bongso, Eng Hin Lee (redaktori). «Stem cells: their definition, classification and sources». Stem Cells: From Benchtop to Bedside. World Scientific, 2005. 5. lpp. ISBN 981-256-126-9. OCLC 443407924.
- ↑ Moore, K.L., T.V.N. Persaud, and A.G. Torchia. Before We Are Born: Essentials of Embryology and Birth Defects. Philadelphia, PA: Saunders, Elsevier. 2013. Print
- ↑ "Stem Cells" Mayo Clinic. Mayo foundation for medical education and research n.d Web. March 23, 2013
- ↑ Jiang Y, Jahagirdar BN, Reinhardt RL, Schwartz RE, Keene CD, Ortiz-Gonzalez XR, Reyes M, Lenvik T, Lund T, Blackstad M, Du J, Aldrich S, Lisberg A, Low WC, Largaespada DA, Verfaillie CM (2002). "Pluripotency of mesenchymal stem cells derived from adult marrow". Nature 418 (6893): 41–9. doi:10.1038/nature00870. PMID 12077603.
- ↑ Ratajczak MZ, Machalinski B, Wojakowski W, Ratajczak J, Kucia M (2007). "A hypothesis for an embryonic origin of pluripotent Oct-4(+) stem cells in adult bone marrow and other tissues". Leukemia 21 (5): 860–7. doi:10.1038/sj.leu.2404630. PMID 17344915.
- ↑ Narasipura SD, Wojciechowski JC, Charles N, Liesveld JL, King MR (2008). "P-Selectin coated microtube for enrichment of CD34+ hematopoietic stem and progenitor cells from human bone marrow". Clin Chem 54 (1): 77–85. doi:10.1373/clinchem.2007.089896. PMID 18024531.
- ↑ Terai S, Ishikawa T, Omori K, Aoyama K, Marumoto Y, Urata Y, Yokoyama Y, Uchida K, Yamasaki T, Fujii Y, Okita K, Sakaida I (2006). "Improved liver function in patients with liver cirrhosis after autologous bone marrow cell infusion therapy". Stem Cells 24 (10): 2292–8. doi:10.1634/stemcells.2005-0542. PMID 16778155.
- ↑ Subrammaniyan R, Amalorpavanathan J, Shankar R, etal (September 2011). "Application of autologous bone marrow mononuclear cells in six patients with advanced chronic critical limb ischemia as a result of diabetes: our experience". Cytotherapy 13 (8): 993–9. doi:10.3109/14653249.2011.579961. PMID 21671823.
- ↑ Madhusankar N. "Use of Bone Marrow derived Stem Cells in Patients with Cardiovascular Disorders". Journal of Stem Cells and Regenerative Medicine.
- ↑ Dedeepiya VD, Rao YY, Jayakrishnan GA, Parthiban JK, Baskar S, Manjunath SR, Senthilkumar R, Abraham SJ (2012). "Index of CD34+ Cells and Mononuclear Cells in the Bone Marrow of Spinal Cord Injury Patients of Different Age Groups: A Comparative Analysis". Bone Marrow Res 2012: 787414. doi:10.1155/2012/787414. PMC 3398573. PMID 22830032.
- ↑ Gardner RL (2002). "Stem cells: potency, plasticity and public perception". Journal of Anatomy 200 (3): 277–82. doi:10.1046/j.1469-7580.2002.00029.x. PMC 1570679. PMID 12033732.
- ↑ Behrens A, van Deursen JM, Rudolph KL, Schumacher B (2014). "Impact of genomic damage and ageing on stem cell function". Nat. Cell Biol. 16 (3): 201–7. doi:10.1038/ncb2928. PMC 4214082. PMID 24576896.
- ↑ «Bone Marrow Transplant». ucsfchildrenshospital.org. Arhivēts no oriģināla, laiks: 2009. gada 4. novembrī. Skatīts: 2016. gada 12. decembrī.
- ↑ Ed Kane. «Stem-cell therapy shows promise for horse soft-tissue injury, disease». DVM Newsmagazine, 2008-05-01. Arhivēts no oriģināla, laiks: 2008-12-11. Skatīts: 2008-06-12.
- ↑ De Coppi P, Bartsch G, Siddiqui MM, Xu T, Santos CC, Perin L, Mostoslavsky G, Serre AC, Snyder EY, Yoo JJ, Furth ME, Soker S, Atala A (2007). "Isolation of amniotic stem cell lines with potential for therapy". Nature Biotechnology 25 (5): 100–106. doi:10.1038/nbt1274. PMID 17206138.
- ↑ «Vatican newspaper calls new stem cell source 'future of medicine' :: Catholic News Agency (CNA)». Catholic News Agency. 2010-02-03. Skatīts: 2010-03-14.
- ↑ «European Biotech Company Biocell Center Opens First U.S. Facility for Preservation of Amniotic Stem Cells in Medford, Massachusetts». Reuters. 2009-10-22. Arhivēts no oriģināla, laiks: 2009-10-30. Skatīts: 2010-03-14.
- ↑ «Europe's Biocell Center opens Medford office – Daily Business Update». The Boston Globe. 2009-10-22. Skatīts: 2010-03-14.
- ↑ «The Ticker». BostonHerald.com. 2009-10-22. Skatīts: 2010-03-14.
- ↑ «Biocell Center opens amniotic stem cell bank in Medford». Mass High Tech Business News. 2009-10-23. Arhivēts no oriģināla, laiks: 2012-10-14. Skatīts: 2012-08-26.
- ↑ «News » World’s First Amniotic Stem Cell Bank Opens In Medford». wbur.org. Skatīts: 2010-03-14.
- ↑ «Biocell Center Corporation Partners with New England's Largest Community-Based Hospital Network to Offer a Unique... – MEDFORD, Mass., March 8 /PRNewswire/». Massachusetts : Prnewswire.com. Skatīts: 2010-03-14.
- ↑ «Making human embryonic stem cells». The Economist. 2007-11-22.
- ↑ Ian Murnaghan for Explore Stem Cells. Updated: 16 December 2013 Why Perform a Stem Cell Transplant?
- ↑ Bone Marrow Transplantation and Peripheral Blood Stem Cell Transplantation In National Cancer Institute Fact Sheet web site. Bethesda, MD: National Institutes of Health, U.S. Department of Health and Human Services, 2010. Cited August 24, 2010
- ↑ Moore, Keith L., T.V.N. Persaud, and Mark G. Torchia. Before We Are Born: Essentials of Embryology and Birth Defects. Philadelphia, PA: Saunders, Elsevier. 2013 Print.
- ↑ Bernadine Healy, M.D.. "Why Embryonic Stem Cells are obsolete" US News and world report. Retrieved on Aug 17, 2015.
- ↑ Stem Cell Basics: What are the potential uses of human stem cells and the obstacles that must be overcome before these potential uses will be realized? Arhivēts 2017. gada 24. februārī, Wayback Machine vietnē.. In Stem Cell Information World Wide Web site. Bethesda, MD: National Institutes of Health, U.S. Department of Health and Human Services, 2009. cited Sunday, April 26, 2009
- ↑ Steinberg, Douglas (November 2000) Stem Cells Tapped to Replenish Organs thescientist.com
- ↑ ISRAEL21c: Israeli scientists reverse brain birth defects using stem cells December 25, 2008. (Researchers from the Hebrew University of Jerusalem-Hadassah Medical led by Prof. Joseph Yanai)
- ↑ Kang KS, Kim SW, Oh YH, Yu JW, Kim KY, Park HK, Song CH, Han H (2005). "A 37-year-old spinal cord-injured female patient, transplanted of multipotent stem cells from human UC blood, with improved sensory perception and mobility, both functionally and morphologically: a case study". Cytotherapy 7 (4): 368–73. doi:10.1080/14653240500238160. PMID 16162459.
- ↑ Strauer BE, Schannwell CM, Brehm M (2009). "Therapeutic potentials of stem cells in cardiac diseases". Minerva Cardioangiol 57 (2): 249–67. PMID 19274033.
- ↑ Stem Cells Tapped to Replenish Organs thescientist.com, Nov 2000. By Douglas Steinberg
- ↑ Hair Cloning Nears Reality as Baldness Cure WebMD November 2004
- ↑ Yen AH, Sharpe PT (2008). "Stem cells and tooth tissue engineering". Cell Tissue Res. 331 (1): 359–72. doi:10.1007/s00441-007-0467-6. PMID 17938970.
- ↑ «Gene therapy is first deafness 'cure'». New Scientist. 2005. gada 14. februāris.
- ↑ «BBC NEWS – UK – England – Southern Counties – Stem cells used to restore vision».
- ↑ Hanson, Charles; Hardarson, Thorir; Ellerström, Catharina; Nordberg, Markus; Caisander, Gunilla; Rao, Mahendra; Hyllner, Johan; Stenevi, Ulf (2013-03-01). "Transplantation of human embryonic stem cells onto a partially wounded human cornea in vitro". Acta Ophthalmologica 91 (2): 127–130. doi:10.1111/j.1755-3768.2011.02358.x. ISSN 1755-3768. PMC 3660785. PMID 22280565.
- ↑ Vastag B (2001). "Stem Cells Step Closer to the Clinic: Paralysis Partially Reversed in Rats with ALS-like Disease". JAMA: The Journal of the American Medical Association 285 (13): 1691–1693. doi:10.1001/jama.285.13.1691. PMID 11277806.
- ↑ Anderson, Querida. «Osiris Trumpets Its Adult Stem Cell Product». Genetic Engineering & Biotechnology News (Mary Ann Liebert, Inc.), 2008-06-15. 13. lpp. Skatīts: 2008-07-06.
(subtitle) Procymal is being developed in many indications, GvHD being the most advanced
- ↑ Gurtner GC, Callaghan MJ, Longaker MT (2007). "Progress and potential for regenerative medicine". Annu. Rev. Med. 58: 299–312. doi:10.1146/annurev.med.58.082405.095329. PMID 17076602. Bone marrow transplantation is, as of 2009, the only established use of stem cells.
- ↑ Hanna V, Gassei K, Orwig KE (2015). "Stem Cell Therapies for Male Infertility: Where Are We Now and Where Are We Going?". Biennial Review of Infertility. Bone marrow transplantation is, as of 2009, the only established use of stem cells.
| Šis ar bioloģiju saistītais raksts ir nepilnīgs. Jūs varat dot savu ieguldījumu Vikipēdijā, papildinot to. |
|