Orbitāļu hibridizācija

Orbitāļu hibridizācija ir enerģētiski izdevīgs process, kad molekulas centrālajā atomā dažāda veida atomārās orbitāles savā starpā kombinējas, veidojot jaunas, citas formas orbitāles ar vienādu formu un enerģiju. Orbitāļu hibridizācijas koncepcija ieņem centrālo vietu valences saišu teorijā, tā ir ļoti noderīga, lai izskaidrotu molekulu ģeometriju.
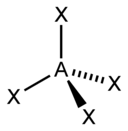
Piemēram, oglekļa atomā četri vērtības elektroni atrodas s un p orbitālēs, konfigurācijā 2s22p2. Kad oglekļa atoms ierosinās, lai veidotu četras ķīmiskās saites, viens no s elektroniem pārvietojas uz p orbitāli, tādējādi šādā atomā ir viens s elektrons un trīs p elektroni konfigurācijā 2s12p3. Tomēr ir noskaidrots, ka tādu vielu kā metāns vai tetrahlorogleklis molekulās visas četras saites ir pilnīgi vienādas, tās pieskaitāmas pie sigma saitēm un ir izvietojušās simetriski, tetraedra formā. Tādēļ pastāv priekšstats par valences orbitāļu hibridizāciju, kad viena s un trīs p orbitāles veido četras hibridizētās sp3 orbitāles. Kvantu mehānikas aprēķini rāda, ka tādām orbitālēm ir nesimetriskas hanteles forma, kam viena puse ir daudz lielāka par otru, un šīs orbitāles telpā ir vērstas uz tetraedra virsotnēm.
Atoma valences elektronu orbitālēm nav obligāti visām jābūt hibridizētām, kombinēties var arī tikai daļa no tām. Ja oglekļa atomā apvienojas viena s orbitāle un divas p orbitāles, notiek sp2 hibridizācija, bet viena p orbitāle saglabā savu sākotnējo simetriskas hanteles formu. Trīs sp2 hibridizētās orbitāles izvietojas plaknes trijstūra formā (ar 120° leņķiem starp orbitālēm) un var veidot trīs sigma saites, bet nehibridizētā p orbitāle var veidot pī saiti ar cita atoma tādu pašu orbitāli. Šādā ceļā veidojas, piemēram, etilēna molekula, kurā starp abiem oglekļa atomiem ir divkāršā saite — viena sigma saite un viena pī saite.
Ja oglekļa atomā apvienojas viena s orbitāle un viena p orbitāle, notiek sp hibridizācija. Šādā gadījumā sākotnējo simetriskas hanteles formu saglabā divas p orbitāles, bet abas sp orbitāles izvietojas lineāri. Tās veido divas sigma saites, bet abas nehibridizētās p orbitāles var veidot divas pī saites ar cita atoma tādām pašām orbitālēm. Šādi veidojas pilnīgi lineārā acetilēna molekula, tajā starp abiem oglekļa atomiem ir trīskāršā saite — viena sigma saite un divas pī saites.
Ja kombinējas viena s, trīs p un viena d orbitāle, notiek sp3d hibridizācija — radušās piecas hibridizētās orbitāles telpā orientētas uz trigonālas bipiramīdas (it kā divas kopā saliktas trijstūra piramīdas) virsotnēm; ja kombinējas viena s, trīs p un divas d orbitāles, notiek sp3d2 hibridizācija un molekulai ar šādu centrālo atomu ir oktaedra forma. Ir arī citi, vēl sarežģītāki hibridizācijas veidi.
Hibridizācijā var piedalīties arī orbitāles, kurās atrodas divi elektroni (nesaistošie elektronu pāri). Piemēram, slāpekļa atomam, tāpat kā oglekļa atomam, ir četras hibridizētās sp3 orbitāles, bet tajās atrodas pieci elektroni, līdz ar to vienā no orbitālēm atrodas divi elektroni un šis pāris saiti neveido. Atlikušie trīs elektroni var veidot sigma saites — tādēļ amonjaka molekulai ir zemas trijstūra piramīdas forma, jo vienu no tetraedra virsotnēm aizņēmis nesaistošais elektronu pāris. Savukārt skābeklim ir jau seši valences elektroni, tam ir divi nesaistošie elektronu pāri, kas aizņem divas tetraedra virsotnes, bet atlikušās kopā ar centrālo atomu veido leņķveida formu. Šādi tiek izskaidrots, kādēļ ūdens molekula ir leņķiska, nevis lineāra.
-
sp3 hibridizētās orbitāles (tetraedra formā)
-
sp2 hibridizētās orbitāles (trijstūra formā)
-
sp hibridizētās orbitāles (lineāras)
Molekulas ģeometrijas atkarība no orbitāļu hibridizācijas
[labot šo sadaļu | labot pirmkodu]Literatūra
[labot šo sadaļu | labot pirmkodu]- Nails Ahmetovs. Neorganiskā ķīmija. Rīga : Zvaigzne, 1978, 60.—63. lpp.
| Vikikrātuvē par šo tēmu ir pieejami multivides faili. Skatīt: hibridizētās orbitāles |