Salicilskābe
| Salicilskābe | |
|---|---|
  Salicilskābes struktūrformula un molekulas modelis | |
| Ķīmiskā formula | C6H4OHCOOH |
| Molmasa | 138,12 g/mol |
| Blīvums | 1440 kg/m3 |
| Kušanas temperatūra | 159 °C |
| Viršanas temperatūra | 211 °C (pie 2666Pa) |
Salicilskābe (2-hidroksibenzoskābe, C6H4OHCOOH) ir bezkrāsaina, kristāliska aromātiskā hidroksikarbonskābe. Salicilskābe ir bezkrāsaini adatveida kristāli ar saldskābu garšu, kas samērā labi šķīst ūdenī.
Salicilskābes molekula satur divas reaģētspējīgas funkcionālās grupas - hidroksilgrupu un karboksilgrupu, tās abas var veidot esterus. Pazīstamākais ir esteris, kur etiķskābe ir reaģējusi ar hidroksilgrupu - acetilsalicilskābe jeb aspirīns.
Atrašanās dabā[labot šo sadaļu | labot pirmkodu]
Salicilskābi satur vītolu miza, no tā arī cēlies vielas nosaukums (latīņu: salix - vītols, kārkls). Salicilskābe pieder pie augu hormoniem.
Iegūšana[labot šo sadaļu | labot pirmkodu]
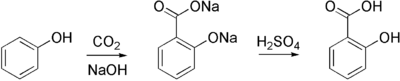
Iegūstot salicilskābi pēc Kolbes - Šmita metodes, autoklāvā sārmainā vidē ogļskābās gāzes atmosfērā no fenola iegūst nātrija salicilātu, ko pēc tam hidrolizē līdz salicilskābei.
Īpašības[labot šo sadaļu | labot pirmkodu]
Ar dzelzs hlorīdu salicilskābe dod violetu krāsojumu.
Reducējot no salicilskābes rodas pimelīnskābe (notiek cikla atvēršanās).
Izmantošana[labot šo sadaļu | labot pirmkodu]
Salicilskābei un tās atvasinājumiem piemīt antiseptiskas īpašības. Lieto medicīnā kā dezinficējošu līdzekli (iekšķīgi - pret locītavu reimatismu) un pārtikas rūpniecībā kā konservantu. Izmanto arī krāsvielu sintēzē.
Skatīt arī[labot šo sadaļu | labot pirmkodu]
| ||||||||
|