Ketēni
- Šis raksts ir par organisku vielu grupu. Par vienkāršāko ketēnu skatīt rakstu ketēns.
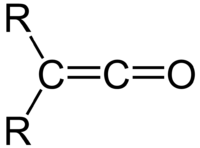
Ketēni ir organiskas vielas, kas satur karbonilgrupu, kura ar dubultsaiti saistīta ar vēl vienu oglekļa atomu (atomu grupējumu >C=C=O). Līdz ar to karbonilgrupas oglekļa atoms ketēnos ir sp hibridizācijas stāvoklī — ar to ketēni atšķiras no ketoniem, kuru molekulās divi aizvietotāji saistīti tieši ar karbonilgrupu. Vienkāršākā ketēna molekulā abi aizvietotāji ir ūdeņraža atomi un šo vielu parasti sauc tāpat par ketēnu (pēc IUPAC nomenklatūras — etenons). Ja ir citi aizvietotāji, ketēnus visbiežāk nosauc saskaņā ar šo aizvietotāju nosaukumiem, piemēram, metilketēns vai difenilketēns. Saskaņā ar IUPAC nomenklatūru ketēnu nosaukumus veido līdzīgi ketonu nosaukumiem, par pamatu ņemot atbilstošā nepiesātinātā ogļūdeņraža nosaukumu un pievienojot izskaņu -ons. Piemēram, metilketēnu pēc IUPAC nomenklatūras dēvē par 1-propenonu.
Ketēnus mēdz iedalīt tādos ketēnos, kam abi aizvietotāji ir ogļūdeņražu atlikumi (ketoketēnos), un tādos, kur viens aizvietotājs ir ūdeņraža atoms (aldoketēnos).
Ketēni ir nestabilas gāzes vai dzeltenīgi šķidrumi ar asu smaku. Ketēni šķīst aromātiskajos ogļūdeņražos un halogēnalkānos. Tiem piemīt izteiktas elektronakceptoras īpašības, pie kam elektrofilais reakcijas centrs ir sp hibridizētais oglekļa atoms.
Ketēniem līdzīga viela ir oglekļa suboksīds O=C=C=C=O.
Ketēniem struktūras ziņā līdzīgas vielas, kuru molekulās skābekļa atoma vietā ir sēra atoms, sauc par tioketēniem. Skābekļa atoma vietā var būt arī trīsvērtīgs slāpekļa atoms — šādus savienojumus sauc par ketēnimīniem, tie satur grupu >C=C=N− un to molekulās ir vēl viens aizvietotājs pie slāpekļa atoma.
Vēsture
[labot šo sadaļu | labot pirmkodu]Ketēnus kā vielu klasi atklājis un pētījis vācu ķīmiķis, Nobela prēmijas laureāts Hermanis Štaudingers.[1]
Iegūšana
[labot šo sadaļu | labot pirmkodu]Ketēnus iegūst, pirolizējot ketonus vai karbonskābes 700—800 °C temperatūrā. Bieži izmanto fosfātu katalizatorus.
- CH3−CO−CH3 → CH2=C=O + CH4
Otra populāra ketēnu iegūšanas metode ir halogēna atšķelšana no α-halogēnkarbonskābju halogenīdiem vai halogēnūdeņraža atšķelšana no karbonskābju halogenīdiem. Šīs reakcijas notiek metālu (piemēram, cinka vai spēcīgu bāzu iedarbībā.
Specifiska ketēnu iegūšanas reakcija ir α-diazoketonu sadalīšana gaismas vai temperatūras iedarbībā (Volfa pārgrupēšanās):
Ķīmiskās īpašības
[labot šo sadaļu | labot pirmkodu]Ketēni ir ķīmiski ļoti aktīvas vielas. Tie kāri reaģē ar dažādiem nukleofiliem reaģentiem, piemēram, ūdeni, veidojot karbonskābju atvasinājumus. Ketēniem ir raksturīgas dimerizācijas reakcijas (veidojas β-laktoni).
Ketēni reaģē ar imīniem, veidojot β-laktāmus (β-laktāmu sintēze pēc Štaudingera):
Izmantošana
[labot šo sadaļu | labot pirmkodu]Ketēnus lieto organiskajā sintēzē kā acetilējošus aģentus. Vienkāršāko ketēnu izmanto rūpniecībā kā starpproduktu etiķskābes un acetanhidrīda iegūšanai no acetona. Ketēni ir starpprodukti penicilīna vai amoksicilīna atvasinājumu sintēzē.
Literatūra
[labot šo sadaļu | labot pirmkodu]- Ojārs Neilands. Organiskā ķīmija. Rīga : Zvaigzne, 1977, 447.—450. lpp.
Atsauces
[labot šo sadaļu | labot pirmkodu]| Vikikrātuvē par šo tēmu ir pieejami multivides faili. Skatīt: ketēni |
- ↑ Hermann Staudinger (1905). "Ketene, eine neue Körperklasse [Ketēni, jauna vielu klase]". Berichte der deutschen chemischen Gesellschaft 38 (2): 1735.—1739. doi:10.1002/cber.19050380283.


