Malonskābe
| Malonskābe | |
|---|---|
  | |
| CAS numurs | 141-82-2 |
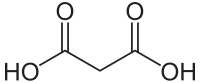
| Ķīmiskā formula | HOOC–CH2–COOH |
| Molmasa | 104,03 g/mol |
| Blīvums | 1631 kg/m3 |
| Kušanas temperatūra | 135 - 137 °C |
| Viršanas temperatūra | sadalās |
Malonskābe (propāndiskābe, metāndikarbonskābe, HOOC–CH2–COOH) ir otrā vienkāršākā divvērtīgā karbonskābe. Malonskābes sāļus un esterus sauc par malonātiem. Malonskābe ir balta, kristāliska viela, kas labi šķīst ūdenī.
Vēsture
[labot šo sadaļu | labot pirmkodu]Malonskābi pirmo reizi ieguva Desenjē 1858. gadā, sadalot ābolskābi oksidētāju klātienē. No tā arī cēlies malonskābes nosaukums (latīņu: malum - ābols).
Atrašanās dabā
[labot šo sadaļu | labot pirmkodu]Dabā malonskābe atrodama, piemēram, biešu sulā (kalcija sāls veidā).
Iegūšana
[labot šo sadaļu | labot pirmkodu]Malonskābi visvieglāk iegūt no etiķskābes, kuru vispirms hlorē līdz monohloretiķskābei CH2Cl–СOOH. Monohloretiķskābe ar kālija cianīdu KCN dod ciānetiķskābi NC–CH2–СOOH, kas sārmainā vidē hidrolizējas līdz malonskābei:
CH2CN–СOOH + 2 H2O → CH2–(СOOH)2 + NH3.
Svarīgākās īpašības
[labot šo sadaļu | labot pirmkodu]Karsējot malonskābe zaudē oglekļa dioksīdu un veido etiķskābi.
CH2(COOH)2 → CO2 + CH3–COOH
Ja malonskābi karsē vakuumā ūdensatņēmēju vielu (P2O5) klātienē, rodas oglekļa suboksīds C3O2, ko dažreiz nekorekti dēvē par malonskābes anhidrīdu.
Malonskābes vidējā metilēngrupa ir ļoti aktīva, jo atrodas starp divām elektronegatīvām karboksilgrupām. Tādēļ malonskābe viegli iesaistās kondensācijas reakcijās ar aldehīdiem un ketoniem, bet malonskābes esteros metilēngrupas ūdeņraža atomi var pat aizvietoties ar sārmu metālu atomiem.
Malonskābe iesaistās kondensācijas reakcijā ar urīnvielu, veidojot barbitūrskābi. Barbitūrskābes atvasinājumus (luminālu, veronālu) lieto medicīnā kā miega līdzekļus.
Izmantošana
[labot šo sadaļu | labot pirmkodu]Malonskābi rūpniecībā izmanto B1 un B2 vitamīnu, kā arī dažu aminoskābju sintēzē.
Patoloģija
[labot šo sadaļu | labot pirmkodu]Ja paaugstinātu malonskābes līmeni pavada paaugstināts metilmalonskābes līmenis, tas var liecināt par bieži neatklātu[1] metabolisku slimību - kombinētu malonskābes un metilmalonskābes acidūriju (CMAMMA).[2] Aprēķinot malonskābes un metilmalonskābes attiecību asins plazmā, CMAMMA var atšķirt no klasiskās metilmalonskābes acidēmijas.[2]
Atsauces
[labot šo sadaļu | labot pirmkodu]- ↑ NIH Intramural Sequencing Center Group; Sloan, Jennifer L; Johnston, Jennifer J; Manoli, Irini; Chandler, Randy J; Krause, Caitlin; Carrillo-Carrasco, Nuria; Chandrasekaran, Suma D et al. (2011-09). "Exome sequencing identifies ACSF3 as a cause of combined malonic and methylmalonic aciduria" (en). Nature Genetics 43 (9): 883–886. doi:10.1038/ng.908. ISSN 1061-4036. PMC PMC3163731. PMID 21841779.
- ↑ 2,0 2,1 Monique G. M. de Sain-van der Velden, Maria van der Ham, Judith J. Jans, Gepke Visser, Hubertus C. M. T. Prinsen, Nanda M. Verhoeven-Duif, Koen L. I. van Gassen, Peter M. van Hasselt. A New Approach for Fast Metabolic Diagnostics in CMAMMA. Berlin, Heidelberg : Springer Berlin Heidelberg, 2016. 15–22. lpp. ISBN 978-3-662-53680-3.
Ārējās saites
[labot šo sadaļu | labot pirmkodu] Vikikrātuvē par šo tēmu ir pieejami multivides faili. Skatīt: Malonskābe.
Vikikrātuvē par šo tēmu ir pieejami multivides faili. Skatīt: Malonskābe.
- Encyclopædia Britannica raksts (angliski)
- Krievijas Lielās enciklopēdijas raksts (krieviski)
| ||||||||
|
