Hidroksilamīns
| Hidroksilamīns | |
|---|---|
 Hidroksilamīna struktūrformula ar starpatomu attālumiem un saišu leņķiem 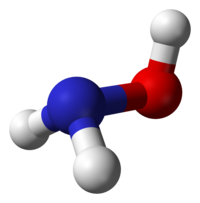 Hidroksilamīna molekulas modelis | |
| Citi nosaukumi | aminols, azanols |
| CAS numurs | 7803-49-8 |
| Ķīmiskā formula | NH2OH |
| Molmasa | 33,030 g/mol |
| Blīvums | 1210 kg/m3 |
| Kušanas temperatūra | 306 K (33 °C) |
| Viršanas temperatūra | 331 K (58 °C) (22 mm Hg spiedienā; sadalās) |
| Šķīdība ūdenī | veido hidrātu |
Hidroksilamīns (NH2OH) ir bezkrāsaina kristāliska (adatveida kristāli) viela, kas viegli šķīst ūdenī, veidojot hidroksilamīna hidrātu NH2OH·H2O. Šķīst arī metanolā un etanolā, nešķīst ēterī. Hidroksilamīns ir higroskopisks un viegli sadalās. Tīri preparāti ir samērā stabili, bet piemaisījumi, it sevišķi sārmi, paātrina sadalīšanos. Hidroksilamīns kūst pie 33 °C, bet pamazām sāk sadalīties jau pie 15 °C. Tālāk sildot izkusušu hidroksilamīnu, tas eksplodē. Strauji ar atklātu liesmu uzkarsējot mēģenē hidroksilamīna pilienu, notiek sprādziens ar šautenes šāvienam līdzīgu troksni.[1]
Vēsture[labot šo sadaļu | labot pirmkodu]
Hidroksilamīnu pirmo reizi ieguva vācu ķīmiķis Vilhelms Losens (Wilhelm Clemens Lossen) hidroksilamīna hidrohlorīda formā 1865. gadā; Losens iedarbojās ar sālsskābi uz alvu etilnitrāta klātienē.[2] Tīrā veidā hidroksilamīnu ieguva 1891. gadā nīderlandiešu ķīmiķis Lobrijs de Bruins {Cornelis Adriaan Lobry van Troostenburg de Bruyn) un franču ķīmiķis Leons Moriss Krismers (Léon Maurice Crismer).[3][4]
Iegūšana[labot šo sadaļu | labot pirmkodu]
Hidroksilamīnu rūpnieciski galvenokārt iegūst tā saucamajā Rašiga procesā, reducējot amonija nitrītu 0 °C temperatūrā ūdens šķīdumā ar HSO3− un SO2, lai iegūtu hidroksilamido-N, N-disulfonāta anjonu:
- NH4NO2 + 2SO2 + NH3 + H2O → 2NH4+ + N(OH)(OSO2)22−
Šo anjonu pēc tam hidrolizē, lai iegūtu hidroksilamonija sulfātu:
- N(OH)(OSO2)22− + H2O → NH(OH)(OSO2)− + HSO4−
- 2NH(OH)(OSO2)− + 2H2O → (NH3OH)2SO4 + SO42−
Tīru NH2OH iegūst, apstrādājot reakcijas produktus ar šķidru amonjaku. Blakusprodukts amonija sulfāts šķidrā amonjakā nešķīst un to var atdalīt nofiltrējot; iztvaicējot amonjaku, paliek ciets hidroksilamīns.
Šveiciešu ķīmiķis Juliuss Tafels (Julius Tafel) atklāja, ka hidroksilamīna hidrohlorīdu vai hidroksilamonija sulfātu var iegūt, elektrolītiski reducējot slāpekļskābi ar sālsskābi vai attiecīgi ar sērskābi[5][6]:
- HNO3 + 3H2 → NH2OH + 2H2O
Hidroksilamīnu var arī iegūt, reducējot slāpekļpaskābi vai kālija nitrītu ar hidrogēnsulfītiem:
- HNO2 + 2HSO3− → N(OH)(OSO2)22− + H2O → NH(OH)(OSO2)− + HSO4−
- NH(OH)(OSO2)− + H3O+ → NH3(OH)+ + HSO4−
Laboratorijās tīru hidroksilamīnu iegūst, destilējot vakuumā hidroksilamīna sāļus.
Molekulas uzbūve[labot šo sadaļu | labot pirmkodu]
Hidroksilamīna molekulu var uzskatīt par amonjaka molekulu, kam viens ūdeņraža atoms aizvietots ar hidroksilgrupu.

Ķīmiskās īpašības[labot šo sadaļu | labot pirmkodu]
Hidroksilamīns ir diezgan eksplozīva viela! |
Hidroksilamīna ķīmiskās īpašības ir samērā līdzīgas hidrazīna īpašībām. Hidroksilamīna ūdens šķīdumam ir sārmaina reakcija. Svaigam šķīdumam nav nekādas smaržas, bet stāvot tas sadalās par ūdeni, amonjaku un slāpekli. Ar skābēm hidroksilamīns viegli veido hidroksilamonija sāļus, vairums no kuriem viegli šķīst ūdenī (nešķīst hidroksilamonija fosfāts un arsenāts).
Hidroksilamīns ir spēcīgs reducētājs. Tas reducē Fēlinga šķīdumu, sārmainā šķīdumā no dzīvsudraba sāļiem izdala brīvu dzīvsudrabu, dzelzi(III) reducē līdz dzelzij(II).
Paskābinātā šķīdumā oksidējas ar bromu līdz slāpekļskābei:
- NH2OH +3Br2 + H2O → HNO3 + 6HBr
Reaģējot ar aldehīdiem un ketoniem, veido oksīmus.
Ir pazīstamas arī reakcijas, kurās hidroksilamīnam ir oksidētāja īpašības, piemēram, tas oksidē sērūdeņradi līdz brīvam sēram:
- NH2OH + H2S → NH3 + S + H2O
Izmantošana[labot šo sadaļu | labot pirmkodu]
Izmanto ķīmijas laboratorijās par reducētāju, lieto arī organiskajā sintēzē. Lieto krāsainajā fotogrāfijā par attīstītāja sastāvdaļu.
Atsauces[labot šo sadaļu | labot pirmkodu]
| Vikikrātuvē par šo tēmu ir pieejami multivides faili. Skatīt: hidroksilamīns |
- ↑ В. А. Палаузов. Химические реактивы. Их свойства, получение, методы испытаний и применение. Харьков, Киев : Государственное научно-техническое издательство Украины, 1935, 230. lpp. (krieviski)
- ↑ W. C. Lossen (1865) "Ueber das Hydroxylamine" (Par hidroksilamīnu), Zeitschrift für Chemie, 8 : 551-553. 551. lpp. teikts: "Ich schlage vor, dieselbe Hydroxylamin oder Oxyammoniak zu nennen." (Es ierosinu nosaukt to par "hidroksilamīnu" vai "oksiamonjaku".)
- ↑ C. A. Lobry de Bruyn (1891) "Sur l'hydroxylamine libre" (Par brīvu hidroksilamīnu), Recueil des travaux chimiques des Pays-Bas, 10 : 100-112.
- ↑ L. Crismer (1891) "Préparation de l'hydroxylamine cristallisée" (Kristalizēta hidroksilamīna iegūšana), Bulletin de la Société chimique de Paris, series 3, 6 : 793-795.
- ↑ Arthur James Hale. The Manufacture of Chemicals by Electrolysis (1st izd.). New York : D. Van Nostrand Co., 1919. 32. lpp. Skatīts: 2014. gada 5. jūnijs.
- ↑ Osswald, Philipp, Geisler, Walter;. Process of preparing hydroxylamine hydrochloride (US2242477). U.S. Patent Office, 1941.
