Kālija cianīds
| Kālija cianīds | |
|---|---|
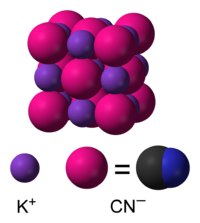 Kālija cianīda kristālrežģis | |
| Citi nosaukumi | ciānkālijs |
| Ķīmiskā formula | KCN |
| Molmasa | 65,12 g/mol |
| Blīvums | 1520 kg/m3 |
| Kušanas temperatūra | 634 °C |
| Viršanas temperatūra | sadalās |
| Šķīdība ūdenī | 71,6g/100ml (25 °C) |
Kālija cianīds (KCN, ciānkālijs) ir ciānūdeņražskābes kālija sāls. Tā ir balta, kristāliska, indīga viela, kas labi šķīst ūdenī. KCN kristāli pēc izskata ļoti atgādina parasto cukuru. Etanolā ciānkālijs šķīst slikti, ogļūdeņražos nešķīst.
Iegūšana
[labot šo sadaļu | labot pirmkodu]Kālija cianīdu var iegūt zilskābes reakcijā ar kālija sārmu:
- HCN + KOH → KCN + H2O
Eksistē arī tiešāka metode, no oglekļa monoksīda, amonjaka un kālija karbonāta dzelzs katalizatora klātienē pie ~600 °C:
- CO + NH3 + K2CO3 → 2KCN + 2H2O + 2CO2
Var iegūt arī, reducējot cianātus; laižot amonjaku pāri izkausētam kālijam un karsējot iegūto kālija amīdu kopā ar ogli; tieši fiksējot slāpekli ar ogles un kālija karbonāta maisījumu.
Īpašības
[labot šo sadaļu | labot pirmkodu]Ciānūdeņražskābe ir ļoti vāja skābe, tāpēc, stāvot gaisā, ciānkālijs un tā šķīdumi reaģē ar gaisa ogļskābo gāzi, izdalot gaisā zilskābi un pārvēršoties par kālija karbonātu. Šī iemesla dēļ ciānkālijs, piekļūstot gaisam, pamazām zaudē toksiskumu.
- 2KCN + CO2 + H2O → K2CO3 + 2HCN
Ciānkālija šķīdumiem ir sārmaina reakcija.
KCN viegli reaģē ar ūdeņraža peroksīdu. Šo reakciju izmanto cianīda ātrai neitralizēšanai, jo radies kālija cianāts ir daudz nekaitīgāka viela.
- KCN + H2O2 → KOCN + H2O
Šķīstošos cianīdus var oksidēt arī ar kālija permanganāta šķīdumu.
Kālija cianīds pieder pie stiprām neorganiskām indēm, tādēļ ar to jāapietas uzmanīgi! |

Kālija cianīda indīgums pamatā ir saistīts ar cianīdjona kompleksēšanas spēju. Cianīdjons viegli veido stabilus kompleksus, kas nobremzē vielmaiņu. Hemoglobīna cianīdkomplekss ir ~100 reizes stabilāks par hemoglobīna kompleksu ar skābekli, tāpēc pēc saindēšanās ar cianīdu asinis vairs nespēj pārnest skābekli. Cianīdi deaktivē arī citus fermentus, piemēram, citohromus, tādēļ šūnas nespēj uzņemt skābekli no asinīm un organisms iet bojā no audu hipoksijas.
Iekļūstot organismā caur gremošanas traktu, cilvēkam nāvējoša deva ir 0,12 g. Ja kuņģis ir piepildīts ar barību, cilvēks var pārciest lielākas devas. Ciānkālijs var iekļūt organismā arī caur ādu, sevišķi, ja tā ir bojāta. Iegremdējot truša ausi 1% KCN šķīdumā, tas iet bojā pēc stundas.
Ilgstošs kontakts ar šķīstošajiem cianīdiem var novest pie hroniskas saindēšanās. Tā izpaužas kā galvassāpes, vispārējs vājums, garšas un ožas traucējumi, aizdusa, nelaba dūša; var būt pastiprināta siekalu un asaru izdalīšanās, akomodācijas traucējumi, potences un dzimumdziņas pavājināšanās, asins sastāva patoloģiskas izmaiņas. Var tikt bojātas nieres, sirds miokards, palielināties vairogdziedzeris; ir novērotas arī paralīzes un psihiski traucējumi. Uzskata, ka cianīdi, ko satur tabakas dūmi, ir smēķējošu sieviešu jaundzimušo bērnu mazāku izmēru un masas cēlonis.[1]
Izmantošana
[labot šo sadaļu | labot pirmkodu]Kālija cianīds ir ļoti stipra inde, tāpēc to agrāk lietoja indēšanai (piemēram, par žurku indi un kukaiņu indēšanai zinātniskiem eksperimentiem, jo tas ātri iedarbojas uz kukaiņiem, un tie nobeidzas bez mehāniskiem bojājumiem).
Cianīdjonu kompleksēšanas spēju lieto arī zelta ieguves rūpniecībā, jo cianīda (tur gan parasti lieto nātrija cianīdu) šķīdums gaisa klātienē šķīdina zeltu. Šādā veidā var izskalot zeltu no zelta rūdas.
- 4 Au + 8 KCN + O2 + 2 H2O → 4 K[Au(CN)2] + 4 KOH
Cianīdus lieto arī dažādu metāla izstrādājumu apzeltīšanā, zelta izstrādājumu tīrīšanai un sudraba spoguļu ražošanā.
Ar ciānkālija šķīdumu var iztīrīt traipus no sudraba nitrāta.
Cianīdus lieto organiskajā sintēzē un farmācijas preparātu ražošanā.
Atsauces
[labot šo sadaļu | labot pirmkodu]- ↑ Вредные химические вещества. Неорганические соединения элементов I-IV групп. Справочник. Л., "Химия", 1988, 343. lpp (krieviski)
Ārējās saites
[labot šo sadaļu | labot pirmkodu] Vikikrātuvē par šo tēmu ir pieejami multivides faili. Skatīt: Kālija cianīds.
Vikikrātuvē par šo tēmu ir pieejami multivides faili. Skatīt: Kālija cianīds.
- Encyclopædia Britannica raksts (angliski)
|
