Akridīns
| Akridīns | |
|---|---|
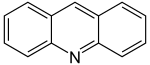  Akridīna struktūrformulas   Akridīna molekulas modeļi | |
| Citi nosaukumi |
dibenz[b,e]piridīns, benz[b]hinolīns, 9-azaantracēns, |
| CAS numurs | 260-94-6 |
| Ķīmiskā formula | C13H9N |
| Molmasa | 179,22 g/mol |
| Blīvums | 1100 kg/m3 |
| Kušanas temperatūra | 107 °C |
| Viršanas temperatūra | 346 °C |
| Šķīdība ūdenī | slikta |
Akridīns (C13H9N) ir heterociklisks slāpekli saturošs organiskais savienojums, kura molekula sastāv no trim kondensētiem cikliem — piridīna cikla, kam abās pusēs atrodas benzola gredzeni. Akridīns ir kristāliska viela (adatveida kristāli) dzeltenā krāsā. Ūdenī vāji šķīstošs. Organiskajos šķīdinātājos šķīst labi, šķīdumiem ir violeta fluorescence. Akridīns ir vāja bāze un ar stiprām neorganiskām skābēm tas veido sāļus, kurus sauc par akridīnija sāļiem.
Vēsture
[labot šo sadaļu | labot pirmkodu]Pirmo reizi ieguvuši vācu ķīmiķi Karls Grēbe (Carl Gräbe) un Heinrihs Karo (Heinrich Caro) 1871. gadā no akmeņogļu darvas.
Iegūšana
[labot šo sadaļu | labot pirmkodu]Akridīnu var iegūt no akmeņogļu darvas vai arī sintētiski. Tas rodas, ciklizējot difenilamīnu vai tā atvasinājumus (N-arilantranilskābes).
Īpašības
[labot šo sadaļu | labot pirmkodu]Skābā vidē veido akridīnija jonu un akridīnija sāļus. Šie sāļi ir ūdenī šķīstoši. Ūdens šķīdumiem piemīt zaļgana fluorescence un spilgti dzeltena krāsa.
Alkilējoties viegli veido ceturtējos sāļus (N-alkilakridīnija sāļus).
Nukleofilās reakcijas notiek pie 9. oglekļa atoma, tajās veidojas akridons un tā atvasinājumi.
Dzīviem organismiem akridīns izraisa hromosomu mutācijas un ir kancerogēna viela.[1]
Izmantošana
[labot šo sadaļu | labot pirmkodu]Svarīgs akridīna atvasinājums ir akrihīns — efektīvs līdzeklis malārijas ārstēšanai.
Akridīnu izmanto arī citu medikamentu un krāsvielu sintēzēm.
Literatūra
[labot šo sadaļu | labot pirmkodu]- O. Neilands. Organiskā ķīmija. Rīga: Zvaigzne, 1977, 724.—725. lpp.
Atsauces
[labot šo sadaļu | labot pirmkodu]| Vikikrātuvē par šo tēmu ir pieejami multivides faili. Skatīt: akridīns |
| Hetero- atomi |
Trīslocekļu cikli | Četrlocekļu cikli | Pieclocekļu cikli | Sešlocekļu cikli | Septiņlocekļu cikli | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| Piesātinātie | Ne- piesātinātie |
Piesātinātie | Ne- piesātinātie |
Piesātinātie | Ne- piesātinātie |
Piesātinātie | Ne- piesātinātie |
Piesātinātie | Ne- piesātinātie | |
| O | Oksirāns | Oksirēns | Oksetāns | Oksets | Tetrahidrofurāns | Furāns | Tetrahidropirāns | Pirāns | Oksepāns | Oksepīns |
| S | Tiirāns | Tiirēns | Tietāns | Tiets | Tetrahidrotiofēns | Tiofēns | Tiāns | Tiīns | Tiepāns | Tiepīns |
| N | Aziridīns | Azirīns | Azetidīns | Azets | Pirolidīns | Pirols Pirolīns Indols*** Karbazols**** |
Piperidīns Hinuklidīns* |
Piridīns Hinolīns*** Izohinolīns*** Akridīns**** |
Azepāns | Azepīns |
| 2O | Dioksetāns | Dioksolāns | Dioksāns | |||||||
| 2N | Diazets | Pirazolidīns Imidazolidīns |
Pirazols Imidazols Pirazolīns Imidazolīns |
Piperazīns | Pirazīns Pirimidīns Piridazīns |
Diazepāns | Diazepīns | |||
| 3N | Triazols Benztriazols*** |
Triazīns | ||||||||
| 4N | Tetrazols | Tetrazīns | ||||||||
| 5N | Pentazols** | |||||||||
| S + N | Tiazolidīns | Tiazols Izotiazols |
Tiomorfolīns | Tiazīns | ||||||
| O + N | Oksaziridīns | Izoksazols Oksazols |
Morfolīns | Oksazīns | ||||||
| O + 2N | Furazāns | Oksadiazīns | ||||||||
- *divi sajūgti sešlocekļu cikli **cikls sastāv tikai no slāpekļa atomiem ***satur kondensētu benzola gredzenu ****satur 2 kondensētus benzola gredzenus
|
