Borskābe
| Borskābe | |
|---|---|
 Borskābes struktūrformula 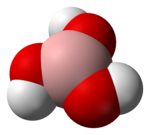 Borskābes molekulas modelis  Pulverveida borskābe | |
| Citi nosaukumi |
ūdeņraža oksoborāts, ortoborskābe, borakskābe, borofaks[1] |
| CAS numurs | 10043-35-3 |
| Ķīmiskā formula | H3BO3 |
| Molmasa | 61,83 g/mol |
| Blīvums | 1435 kg/m3 |
| Kušanas temperatūra | 170,9 °C |
| Viršanas temperatūra | 300 °C |
| Šķīdība ūdenī |
2,52 g/100 mL (0 °C) 4,72 g/100 mL (20 °C) 5,7 g/100 mL (25 °C) 19,10 g/100 mL (80 °C) 27,53 g/100 mL (100 °C) |
Borskābe jeb ortoborskābe (H3BO3 vai B(OH)3) ir ļoti vāja neorganiska skābe. Borskābe ir cieta bezkrāsaina viela, tās triklīnie, slāņainie kristāli ir plānu zvīņu veidā, kuras taustot liekas taukainas. Tas saistīts ar borskābes kristālrežģa uzbūvi, kur molekulas saistītas savā starpā ar ūdeņraža saitēm plakanos monomolekulāros slāņos, bet šos slāņus savā starpā saista daudz vājākie starpmolekulārie spēki. Ūdenī šķīst diezgan slikti, bet šķīdība strauji pieaug līdz ar temperatūras paaugstināšanos. Borskābei šķīstot, tiek uzņemts siltums,[2] tādēļ šķīdums atdziest. Borskābes sāļus sauc par borātiem.
Vēsture
[labot šo sadaļu | labot pirmkodu]Borskābi ieguva holandiešu natūrfilozofs Vilhelms Hombergs (Wilhelm Homberg) 1702. gadā, karsējot boraku kopā ar sērskābi.[3] To drīz sāka pielietot medicīnā ar nosaukumu sal sedavitum.
Atrašanās dabā
[labot šo sadaļu | labot pirmkodu]Borskābe dabā atrodama reta minerāla sasolīna veidā. Tā atrodama minerālūdeņu sastāvā, kā arī karstajos avotos un vulkāniskajās fumarolās (vieglās gaistamības kopā ar ūdens tvaikiem dēļ). Nenozīmīgos daudzumos borskābi satur augļi, ogas, apiņi, dažreiz vīns.
Iegūšana
[labot šo sadaļu | labot pirmkodu]Ortoborskābi iegūst, hidrolizējot bora halogenīdus, borānus un citus savienojumus. Rodas, pievienojot stipras skābes borātu šķīdumiem. Polimērās borskābes, kā tetraborskābi, atsevišķi brīvā veidā izdalīt praktiski nav iespējams.
Īpašības
[labot šo sadaļu | labot pirmkodu]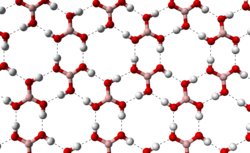
Karsējot ortoborskābe atšķeļ ūdeni un pārvēršas par metaborskābi HBO2. Metaborskābe ir bezkrāsaina kristāliska viela, kam pazīstamas trīs modifikācijas — kubiskā jeb γ-HBO2 (visstabilākā); monoklīnā jeb β-HBO2 un rombiskā jeb α-HBO2.
Tālāk karsējot, metaborskābe vispirms pakāpeniski pāriet tetraborskābē H2B4O7 un pēc tam zaudē visu ūdeni, rodoties bora oksīdam B2O3 jeb borskābes anhidrīdam.
Ūdens šķīdumos borskābe eksistē dažādu poliborskābju ar vispārīgo formulu Н3m-2nВmО3m-n veidā. Neitralizējot borskābes šķīdumus ar sārmiem, arī rodas nevis ortoborāti, bet metaborāti, tetraborāti un citi poliborāti. Pazīstamākais borskābes sāls ir nātrija tetraborāts Na2B4O7·10H2O jeb boraks.
Borskābes šķīdumu skābās īpašības, atšķirībā no citām skābēm, nodrošina nevis protonu (H+) atšķelšana, bet gan hidroksiljonu (OH−) pievienošana:
- B(OH)3 + H2O ⇄ [B(OH)4]− + H+
Borskābe ir ļoti vāja skābe, kuru no sāļu šķīdumiem izspiež vairums citu skābju. Borskābei piemīt arī nelielas amfotēras īpašības, piemēram, ir pazīstams nestabils bora hidrogēnsulfāts В(HSO4)3.
Karsējot borskābe šķīdina metālu oksīdus, veidojot sāļus.
Ar spirtiem koncentrētas sērskābes klātienē veido esterus:
Borskābes metilestera veidošanās ir kvalitatīva analītiska reakcija borskābes un borātu noteikšanai. Aizdedzinot borskābes metilesteris sadeg ar skaistu zaļu liesmu.
Tā kā borskābe reaģē ar silikātiem, veidojot kompleksus borsilikātus, ko viegli sadalīt ar sālsskābi, šo reakciju izmanto analītiskajā ķīmijā silikātu noteikšanai.[4]
Borskābe ir toksiska viela, tās nāvējošā deva pieaugušam cilvēkam ir 15—20 g.[5] Akūti saindējoties, rodas nelabums, stipra vemšana, caureja, sāpes vēderā; vēlāk izsitumi, ādas lobīšanās. Borskābei piemīt hepatotoksiska, gonadotropa, holinolītiska iedarbība; tā viegli pārvar placentāro barjeru, tādēļ īpaši jāuzmanās grūtniecēm. Ir aprakstīti saindēšanās gadījumi (tai skaitā letāli), borskābei uzsūcoties caur bojātu vai nebojātu ādu, it īpaši bērniem.[6] Tā kā borskābe samērā lēni tiek izvadīta caur nierēm, tā var kumulēties (uzkrāties) organismā, izraisot hronisku saindēšanos.
Izmantošana
[labot šo sadaļu | labot pirmkodu]Borskābi jau no 19. gadsimta 60. gadiem izmanto medicīnā par dezinficējošu līdzekli, kas nekairina brūces un kam nav krāsas, smaržas un garšas. Mūsdienu medicīnā tiek uzskatīts, ka borskābes pretmikrobu aktivitāte ir zema. Tās toksiskuma dēļ (ietekmē CNS, asinsriti, var pat izraisīt akūtu nieru mazspēju) bērnu ārstēšanā borskābi izmantot nedrīkst (aizliegts izmantot bērnu un grūtnieču ārstēšanā jau PSRS laikā 1987. gadā). Borskābi ar nosaukumu Acidum boricum medicīnā lieto kā pulvera veidā, tā arī ūdens vai spirta šķīdumos, kā arī 5—10% ziedes veidā. Lieto dažu ādas slimību ārstēšanai, acu skalošanai, mutes un kakla skalošanai iekaisumu gadījumos.[7]
Borskābi un boraku izmanto stikla (borsilikātstiklu — pireksa un Jēnas stikla) un keramikas ražošanā; koksnes piesūcināšanai; par boru saturošu augu mēslojumu. Borskābe ir citu bora savienojumu iegūšanas izejviela. Laboratorijās borskābi lieto buferšķīdumu pagatavošanai, bet fotogrāfijā — smalkgraudainu attīstītāju un skābo fiksāžu sastāvā. Lieto arī par kusni zeltu saturošu juvelierizstrādājumu lodēšanā, sveču izgatavošanā dakts stingrības nodrošināšanai, ādu miecēšanā.
Novusa spēlē borskābi tradicionāli izmanto galdiņa apstrādei labākai kauliņu slīdamībai.[8]
Pārtikas rūpniecībā borskābi ierobežoti izmanto par konservantu E284 (produktiem, kas netiek patērēti lielos daudzumos, piemēram, kaviāram).
2010. gadā ar EK regulu borskābes tirdzniecība Latvijā tika ierobežota.[9][10]
Atsauces
[labot šo sadaļu | labot pirmkodu]- ↑ «MK noteikumi Nr. 86». Arhivēts no oriģināla, laiks: 2016. gada 5. martā. Skatīts: 2014. gada 29. decembrī.
- ↑ N. Ahmetovs. Neorganiskā ķīmija. R:, Zvaigzne, 1978, 491. lpp.
- ↑ Г. Реми. Курс неорганической химии. Том I. Москва : Издательство иностранной литературы, 1963, 360. lpp. (krieviski)
- ↑ Г. Реми. Курс неорганической химии. Том I. Москва, Издательство иностранной литературы, 1963, lpp. 374. (krieviski)
- ↑ Вредные химические вещества. Неорганические соединения элементов I-IV групп. Справочник. Л., "Химия", 1988, 194. lpp. (krieviski)
- ↑ Вредные химические вещества. Неорганические соединения элементов I-IV групп. Справочник. Л., "Химия", 1988, 197. lpp. (krieviski)
- ↑ Indulis Purviņš, Santa Purviņa. Praktiskā farmakoloģija. R:, Zāļu infocentrs, 2011, 656. lpp. ISBN 978-9984-854-20-5
- ↑ «Novusa spēlētāji sašutuši par borskābes tirgošanas aizliegumu». Arhivēts no oriģināla, laiks: 2016. gada 7. martā. Skatīts: 2014. gada 29. decembrī.
- ↑ «Veselības inspekcija brīdina par borskābes bīstamību». Arhivēts no oriģināla, laiks: 2014. gada 1. septembrī. Skatīts: 2014. gada 29. decembrī.
- ↑ Borskābe aizliegta. Kas nākamais?
Ārējās saites
[labot šo sadaļu | labot pirmkodu] Vikikrātuvē par šo tēmu ir pieejami multivides faili. Skatīt: Borskābe.
Vikikrātuvē par šo tēmu ir pieejami multivides faili. Skatīt: Borskābe.
- Encyclopædia Britannica raksts (angliski)
|
