Etanols
| Etanols | |
|---|---|
 Etanola struktūrformulas  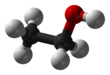 Etanola molekulas modeļi | |
| Citi nosaukumi | etilspirts, metilkarbinols |
| CAS numurs | 64-17-5 |
| Ķīmiskā formula | C2H5OH |
| Molmasa | 46,07 g/mol |
| Blīvums | 789 kg/m3 |
| Kušanas temperatūra | 158,8 K (-114,3 °C) |
| Viršanas temperatūra | 351,6 K (78,4 °C) |
| Šķīdība ūdenī | jaucas jebkurās attiecībās |
Etanols (etilspirts, metilkarbinols, CH3CH2OH, EtOH) ir plašāk pazīstamais spirts. Ļoti bieži ar jēdzienu spirts saprot tieši etanolu. Etanols ir neirotoksiska psihoaktīva viela, kas ir alkoholisko dzērienu galvenā sastāvdaļa.[1] Etanolu izmanto arī kā šķīdinātāju, antiseptiķi, degvielu, un arī modernajos termometros. Etanols ir mazviskozs, caurspīdīgs, degtspējīgs šķidrums ar raksturīgu spirta smaržu. Etanols ļoti labi šķīst ūdenī (sajaucas jebkurās attiecībās). Empīriskajai formulai C2H6O atbilst vēl viens izomērs CH3OCH3 — dimetilēteris, kas parastos apstākļos ir gāze.

Iegūšana[labot šo sadaļu | labot pirmkodu]
Etanolu var iegūt ar bioķīmiskām metodēm (raudzējot ogļhidrātus) vai arī ķīmiski, parasti — hidratējot etilēnu:
- CH2CH2 + H2O → CH3CH2OH
Ir arī citas metodes, taču tās ir dārgākas.
Izmantošana[labot šo sadaļu | labot pirmkodu]
Etanolu lieto kā šķīdinātāju, un tas arī ir visu alkoholisko dzērienu sastāvdaļa. Organismā etanols, tāpat kā citi vienvērtīgie pirmējie spirti, noārdās, vispirms oksidējoties par aldehīdu (šajā gadījumā — acetaldehīdu) un tālāk par karbonskābēm, oglekļa dioksīdu un ūdeni. No atjaunīgajiem energoresursiem iegūts etanols tiek izmantots arī kā alternatīva degviela autotransporta nozarē.
Farmakoloģija[labot šo sadaļu | labot pirmkodu]

Ietekme uz centrālo nervu sistēmu[labot šo sadaļu | labot pirmkodu]
Etanols nomāc centrālo nervu sistēmu, tam pie subletālām devām ir būtiska psihoaktīva ietekme. Tā kā etanols spēj mainīt cilvēka apziņu, tas tiek uzskatīts par psihotropo vielu. Nāve no etanola ir iespējama tad, kad alkohola līmenis asinīs sasniedz 0,4%. Līmenis asinīs 0,5% vai vairāk ir parasti nāvējošs. Līmenis, mazāks nekā 0,1%, var izraisīt saindēšanos, bet bezsamaņa bieži rodas pie 0,3—0,4%.[2]
Etanola daudzumu organismā parasti kvantitatīvi apzīmē promilēs. Tabulā apkopoti simptomi atkarībā no etanola patēriņa. Mazās devās etanols rada eiforiju un atslābināšanos; cilvēks mēdz kļūt runīgāks, uzlabojas garastāvoklis, un var pieņemt nepareizus lēmumus. Pie lielākām devām etanols darbojas nomācoši uz centrālo nervu sistēmu, zūd sāpju izjūta, rodas miegainība. Lielākās devās tiek traucēta maņu un kustību funkcija, palēnināta reakcija un refleksi, veidojas neziņa, bezsamaņa. Galējās devās tiek nomāktas iegarenās smadzenes un to elpošanas un vazomotorais centrs, kas izraisa elpošanas un sirdsdarbības apstāšanos.[3]
Etanols iedarbojas uz centrālo nervu sistēmu, galvenokārt saistoties ar GABA A (gamma-aminosviestskābes) receptoriem, pastiprinot nomākšanas neirotransmitera GABA efektu.[4]
Ilgstoša alkohola lietošana var radīt būtiskus, paliekošus smadzeņu u.c. orgānu bojājumus.
Pārtraucot lietot alkoholu pēc vairāku gadu lietošanas, var būt nāvīgas sekas, var rasties arī trauksmainība, veģetatīvā disfunkcija, krampji un halucinācijas. Delīrijs ir raksturīgs cilvēkiem ar ilgu dzeršanas vēsturi.
| Promiles | Simptomi [5] |
|---|---|
| 0,5 | Eiforija, atslābinātība, runīgums |
| 1 | Centrālās nervu sistēmas nomākšana, slikta dūša, vemšana, traucēta kustības un maņu funkcija, apziņas traucējumi |
| >1,4 | Samazināta asins plūsma uz smadzenēm |
| 3 | Iespējams samaņas zudums |
| 4 | Iespējama nāve |
| >5,5 | Nāve |
Etanols ir konstatējams arī atturībnieku asinīs — ap 0,02 promilēm.[3]
| Izdzertā alkohola daudzums, ml | Nomāktie CNS rajoni | Darbības stadija |
|---|---|---|
| 100-300 | Garoza | Eiforija un uzbudinājums |
| 300-600 | Garoza, zemgaroza, muguras smadzenes | Narkoze |
| 600-1000 | Garoza, zemgaroza, muguras smadzenes, iegarenās smadzenes | Agonālā |
| virs 1000 | Visi | Nāve |
Ietekme uz aknu stāvokli[labot šo sadaļu | labot pirmkodu]
Aknu slimību risks paaugstinās, ja etanola lietošana pārsniedz 20—30 g dienā sievietēm un 40—60 g dienā vīriešiem. Aknu ciroze ir tikai aptuveni 10% alkohola lietotāju. Alkohola aknu bojājums ir daudzfaktoru slimība, tās attīstību nosaka ne tikai pārlieku liels alkohola patēriņš, bet arī dzimums, ģenētika un citas aknu slimības. Alkohola hepatīts (aknu iekaisums) attīstās arī tikai nelielai daļai pacientu, kas lieto pārmērīgi daudz alkohola. Taču pat pārtraucot alkohola lietošanu un uzsākot adekvātu ārstēšanu, 28 dienu mirstība ir augsta (30—50%). Savukārt alkohola izraisītas taukainās hepatozes gadījumā prognoze ir laba, ja pacients pārtrauc alkohola lietošanu.[6]
Ietekme uz ogļhidrātu maiņu[labot šo sadaļu | labot pirmkodu]
Etanols hroniskiem alkoholiķiem var izraisīt alkohola hipoglikēmiju jeb stāvokli, kad asinīs ir zems cukura līmenis. Tas vairāk raksturīgs tiem, kas pēc izteiktas alkohola lietošanas vairākas dienas neēd un, etanolam bloķējot glikoneoģenēzi, organisms vairs nespēj asinīs uzturēt pietiekamu glikozes līmeni.[3]
Zāļu līdzekļu mijiedarbība[labot šo sadaļu | labot pirmkodu]
Etanols var pastiprināt medikamentu nomierinošo iedarbību un nomākt centrālo nervu sistēmu, piemēram, kombinējot ar barbiturātiem, opioīdiem, sedatīvajiem antihistamīniem un antidepresantiem.[7][3] Lietojot alkoholu ar marihuānu, alkohols var paaugstināt marihuānas aktīvās vielas THC līmeni. Mijiedarbojoties ar amfetamīniem, var izraisīt izteikti paaugstinātu asinsspiedienu.[3]
B1 hipovitaminoze[labot šo sadaļu | labot pirmkodu]
Hroniska etanola lietošana var izraisīt B1 hipovitaminozi, kas savukārt izraisa Vernikes encefalopātiju, kas ir izplatītākā tiamīna trūkuma izpausme rietumu pasaulē. Tā izpaužas ar apziņas un īslaicīgās atmiņas zudumiem, dezorientāciju, halucinācijām, līdzsvara traucējumiem. Ar šo slimību slimo ap 1% populācijas, galvenokārt alkoholiķi. Tās uzliesmojuma periodā, nepietiekami kontrolējot vitamīna deficītu, nāvējošs iznākums ir apmēram 20% gadījumu.[3]
Bieža urinēšana[labot šo sadaļu | labot pirmkodu]
Etanols ietekmē antidiurētisko hormonu izstrādāšanos, kuru funkcija ir saistīta ar ūdens aizturi ķermenī. Tādējādi netieši etanols samazina spēju reabsorbēt ūdeni nieru kanāliņos, līdz ar to dzēris cilvēks biežāk izjutīs vajadzību urinēt.[8]
Alkohola izdale[labot šo sadaļu | labot pirmkodu]
Lielākā daļa alkohola oksidējas un izdalās ogļskābās gāzes un ūdens veidā. Neliela daļa (mazāk par 1%) izdalās ar urīnu un 1—3% ar izelpojamo gaisu. Alkohols organismā tiek noārdīts pastāvīgā ātrumā, kuru gandrīz nav iespējams ietekmēt. Liels daudzums augļu cukura mazliet palielina alkohola noārdīšanās ātrumu aknās. Turklāt liels alkohola patēriņš izraisa tā saucamo metabolisko toleranci, kuras rezultātā alkohola noārdīšanās ātrums var palielināties gandrīz divas reizes.[9]
Resnās zarnas baktērijas vielmaiņas ceļš[labot šo sadaļu | labot pirmkodu]
Daļa zarnu trakta mikroorganismu satur enzīmu alkohola dehidrogenāzi, kuru izmantojot, tie spēj bezskābekļa apstākļos rūgšanas reakcijā pārveidot cukuru par etanolu, vienlaikus saņemot no šīs reakcijas enerģiju. Alkohola dehidrogenāzes katalizētā rūgšana tomēr ir atgriezeniska, un, tā kā tajā dominē liels etanola daudzums, alkohola dehidrogenāze sāk metabolizēt etanolu un ražot acetaldehīdu.
Radies acetaldehīds tālāk var oksidēties par etiķskābi vai nu ar baktēriju, vai ar aldehīda dehidrogenāzes, kuru satur zarnu trakta gļotādas šūnas, palīdzību. Daļa no zarnu traktā esošā acetaldehīda caur portālo asinsriti var uzsūkties aknās un tur tālāk oksidēties par etiķskābi. [10][11][9]
Denaturēšana[labot šo sadaļu | labot pirmkodu]
Lai citiem mērķiem paredzēto (un tādēļ ar akcīzes nodokli neaplikto un lētāko) etanolu cilvēki nemēģinātu izmantot dzeršanai, to speciāli padara nedzeramu, piejaucot vai nu indīgas vielas, kas netraucē etanola tiešiem izmantošanas mērķiem (metanols, kam ir gandrīz identiskas īpašības; formalīns; piridīna bāzes), vai nu vielas, kas piešķir spirtam ļoti nepatīkamu smaržu un garšu (tostarp piridīna bāzes), kā arī etanols tiek iekrāsots. Šādu apstrādāšanu sauc par denaturēšanu, bet iegūto produktu – par denaturēto spirtu.[12]
Atsauces[labot šo sadaļu | labot pirmkodu]
| Vikikrātuvē par šo tēmu ir pieejami multivides faili. Skatīt: etanols |
- ↑ "10th Special Report to the U.S. Congress on Alcohol and Health: Highlights from Current Research". National Institute of Health. National Institute on Alcohol Abuse and Alcoholism. June 2000. p. 134. Retrieved 21 October 2014.
The brain is a major target for the actions of alcohol, and heavy alcohol consumption has long been associated with brain damage. Studies clearly indicate that alcohol is neurotoxic, with direct effects on nerve cells. Chronic alcohol abusers are at additional risk for brain injury from related causes, such as poor nutrition, liver disease, and head trauma.
- ↑ David A. Yost (2002). Acute care for alcohol intoxication. 112. Postgraduate Medicine Online. Arhivēts no oriģināla 2010. gada 14. decembrī. Atjaunināts: 2015. gada 7. martā.
- ↑ 3,0 3,1 3,2 3,3 3,4 3,5 3,6 Indulis Purviņš, Santa Purviņa (2002). Praktiskā farmakoloģija (3. izd.). Rīga: Zāļu infocentrs. 174. lpp. ISBN 9984193313 Nepareizs ISBN.
- ↑ Santhakumar V, Wallner M, Otis TS (2007). "Ethanol acts directly on extrasynaptic subtypes of GABAA receptors to increase tonic inhibition". Alcohol 41 (3): 211–21?. doi:10.1016/j.alcohol.2007.04.011. PMC 2040048. PMID 17591544.
- ↑ Pohorecky LA, Brick J (1988). "Pharmacology of ethanol". Pharmacol. Ther 36 (2–3): 335–427.
- ↑ «Arhivēta kopija». Arhivēts no oriģināla, laiks: 2016. gada 4. martā. Skatīts: 2016. gada 9. janvārī.
- ↑ Yost, David A. (2002). "Acute care for alcohol intoxication" 112 (6). Postgraduate Medicine Online.
- ↑ Mechanism of Dehydration Following Alcohol Ingestion KATHLEEN E. ROBERTS, MD Arch Intern Med.1963;112(2):154-157. doi:10.1001/archinte.1963.03860020052002 http://archinte.jamanetwork.com/article.aspx?articleid=568848 Arhivēts 2015. gada 8. janvārī, Wayback Machine vietnē.
- ↑ 9,0 9,1 Narkoloģija. Mikko Salaspuro, Astrīda Stirna, Inga Landsmane, Sarmīte Skaida, Ilze Stankeviča
- ↑ Microbial metabolism of ethanol and acetaldehyde and clinical consequences. M.Salaspuro http://onlinelibrary.wiley.com/doi/10.1080/13556219772840/abstract
- ↑ Aldehyde dehydrogenase activity and acetate production by aerobic bacteria representing the normal flora of human large intestine. Nosova T1, Jokelainen K, Kaihovaara P, Jousimies-Somer H, Siitonen A, Heine R, Salaspuro M. http://www.ncbi.nlm.nih.gov/pubmed/9010546
- ↑ Степаненко, Б. М. Органическая химия. Медгиз:Москва, 1951.— с. 118.
| ||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||
|

