Bors
- Šis raksts ir par ķīmisko elementu. Par citām jēdziena Bors nozīmēm skatīt nozīmju atdalīšanas lapu.
| Bors | |||||||
|---|---|---|---|---|---|---|---|
| |||||||
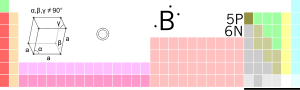
 Kristālisks bors | |||||||
| Oksidēšanas pakāpes | +4, +3, +2, +1 | ||||||
| Elektronegativitāte | 2,04 | ||||||
| Blīvums | 2460 kg/m3 | ||||||
| Kušanas temperatūra | 2349 K (2076 °C) | ||||||
| Viršanas temperatūra | 4200 K (3927 °C) | ||||||
Bors ir ķīmiskais elements ar simbolu B un atomskaitli 5. Bors dabā ir sastopams galvenokārt borskābes H3BO3 sāļu veidā, pazīstamākais šāds sāls ir nātrija tetraborāta dekahidrāts (nātrija tetraborāts ar 10 ūdens molekulām) Na2B4O7·10H2O (boraks). Tīrā veidā bors ir cieta kristāliska viela. Boram ir iespējamas vairākas alotropiskās formas. Amorfais bors ir brūns pulveris, kristāliskais bors ir cieta, melna, kristāliska viela. Bora nitrīds (BN) ir viena no cietākajām pazīstamajām vielām. Savienojumos bors parasti ir trīsvērtīgs.
Īpašības[labot šo sadaļu | labot pirmkodu]
Reducējot bora savienojumus, parasti iegūst amorfo boru. Kristāliskajam boram ir iespējamas vairākas kristāliskās formas. Izplatītākās ir alfa un beta trigonālās formas, un tetragonālā forma.
Kristāliskais bors laiž cauri infrasarkano starojumu. Kristāliskajam boram zemās temperatūrās ir diezgan maza elektrovadītspēja, bet tā palielinās, paaugstinot temparatūru.
Bors ir elektrofils, jo tam ir daudz neaizpildītu orbitāļu. Daudzi bora savienojumi ir Lūisa skābes, tie iesaistās reakcijās ar savienojumiem, kas satur daudz elektronu (nukleofiliem). Šādas reakcijas ir raksturīgas organiskajiem savienojumiem. Bors ir arī nemetāls ar vismazāko elektronegativitāti, tāpēc reakcijās tas parasti oksidējas (zaudē elektronus). Bors, tāpat kā ogleklis, spēj veidot stabilas kovalentās saites. Ogļūdeņražiem analogie borūdeņraži (borāni) gan ir mazāk stabili. Tos dažreiz lieto raķešdegvielām.
Savienojumi[labot šo sadaļu | labot pirmkodu]
Nozīmīgākie bora savienojumi ir:
- Boraks - nātrija tetraborāta dekahidrāts Na2B4O7·10H2O. Viena no galvenajām bora un citu bora savienojumu izejvielām. To lieto arī par korozijas inhibitoru.
- Nātrija tetraborāta pentahidrāts Na2B4O7·5H2O. Viena no galvenajām borsilikātu stikla un nātrija perborātu balinātāju izejvielām.
- Borskābe H3BO3 - lieto par izejvielu dažu sastāvu borsilikātu stikliem (ar samazinātu sārmu saturu), kā arī medicīnā. Borskābi lieto arī, lai samazinātu kokvilnas audumu degamību. Borskābi lieto arī uz novusa galdiem, lai mazinātu to berzi.
- Bora nitrīds BN. Tam ir vairākas alotropiskās formas. Viena no tām pēc struktūras ir analoga dimantam (borazons). Tā ir viena no cietākajām pazīstamajām vielām un to lieto par abrazīvu. Lai arī tas ir mīkstāks par dimantu, tam ir labāka karstumizturība.
Boru un tā savienojumus lieto arī pirotehnikā, jo bors iekrāso liesmu zaļā krāsā; koksnes konservantiem, jo tie ir mazāk toksiski kā hroma savienojumi un ogļu darva; par leģējošo elementu pusvadītāju ražošanā (p tipa pusvadītājiem); izotopu 10B lieto, lai strauji apturētu kodolreaktorus avārijas situācijās, jo šis izotops labi absorbē neitronus un nobremzē kodolreakcijas.
Ārējās saites[labot šo sadaļu | labot pirmkodu]
 Vikikrātuvē par šo tēmu ir pieejami multivides faili. Skatīt: Bors.
Vikikrātuvē par šo tēmu ir pieejami multivides faili. Skatīt: Bors.
- Latvijas Nacionālās enciklopēdijas šķirklis
- Encyclopædia Britannica raksts (angliski)
- Brockhaus Enzyklopädie raksts (vāciski)
- Krievijas Lielās enciklopēdijas raksts (krieviski)
- Encyclopædia Universalis raksts (franciski)
| H | He | ||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | As | Br | Kr | ||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Te | I | Xe | |||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Rn | ||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| Sārmu metāli | Sārmzemju metāli | Lantanīdi | Aktinīdi | Pārejas metāli | Citi metāli | Pusmetāli | Citi nemetāli | Halogēni | Cēlgāzes |
|